题目内容
11.海洋是地球上最大的储水库,浩瀚的海洋蕴藏着丰富的化学资源.(1)目前世界上60%的镁是从海水中提取的.其主要步骤如图:

①提取Mg的过程中,试剂A可以选用氢氧化钠溶液,试剂B选用稀盐酸,由无水MgCl2制取Mg的基本反应类型为分解反应.
②分离出Mg(OH)2后的NaCl溶液中还含有CaCl2、Na2SO4等杂质,为了获得NaCl溶液,在分离后的溶液中依次加入过量的BaCl2溶液、Na2CO3溶液,过滤,再向滤液中加入适量盐酸.实验中加入过量BaCl2溶液是为了除去Na2SO4;加入过量Na2CO3溶液的目的是除去CaCl2和BaCl2.
(2)从海水中制得的氯化钠除可以食用外,还常用作工业原料生产相应的化工产品,如工业上利用氯化钠和水在通电条件下生成烧碱、氢气和氯气,试写出上述化学方程式:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
分析 (1)①氢氧化钙能和硫酸镁反应生成氢氧化镁沉淀和硫酸钙;氢氧化镁能和稀盐酸反应生成氯化镁和水;电解氯化镁生成镁和氯气;
②氯化钡能和硫酸钠反应生成硫酸钡沉淀和氯化钠,碳酸钠能和氯化钙反应生成碳酸钙沉淀和氯化钠以及碳酸钠和氯化钡反应生成碳酸钡和氯化钠;
根据反应物和生成物及其质量守恒定律可以正确书写化学方程式.
解答 解:(1)①提取镁的过程中,试剂A可以选用氢氧化钠,因为由硫酸镁反应生成氢氧化镁,根据复分解反应的原理,硫酸镁是与可溶性碱发生反应;氢氧化镁为不溶性碱,变成氯化镁,试剂是选用稀盐酸;电解氯化镁生成镁和氯气,一种物质生成两种物质,符合分解反应特点,属于分解反应;故填:氢氧化钠溶液,稀盐酸,分解反应;
②要除去氯化钠中的CaCl2、Na2SO4等杂质,可以首先加入氯化钡溶液除去硫酸钠,加入的碳酸钠溶液能与氯化钙溶液反应生成碳酸钙沉淀,能与上一步中多加的氯化钡反应生成碳酸钡沉淀,所以实验中加入过量BaCl2溶液是为了除去硫酸钠;加入过量Na2CO3溶液的目的是除去CaCl2和BaCl2.故填:Na2SO4;除去CaCl2和BaCl2;
(2)氯化钠和水在通电条件下生成烧碱、氢气和氯气的化学方程式为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,故填:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
点评 本题主要考查海水中提取镁的知识,解答时应该充分理解物质之间相互作用反应的情况.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.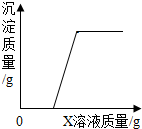 向稀盐酸和硫酸铜的混合溶液中逐滴滴入X溶液至过量,生成沉淀的质量随滴入溶液质量的变化关系如图所示.则X可能是( )
向稀盐酸和硫酸铜的混合溶液中逐滴滴入X溶液至过量,生成沉淀的质量随滴入溶液质量的变化关系如图所示.则X可能是( )
 向稀盐酸和硫酸铜的混合溶液中逐滴滴入X溶液至过量,生成沉淀的质量随滴入溶液质量的变化关系如图所示.则X可能是( )
向稀盐酸和硫酸铜的混合溶液中逐滴滴入X溶液至过量,生成沉淀的质量随滴入溶液质量的变化关系如图所示.则X可能是( )| A. | 硝酸银溶液 | B. | 氯化钡溶液 | C. | 硝酸钾溶液 | D. | 氢氧化钠溶液 |
2.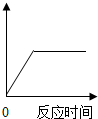 在实验室加热氯酸钾和二氧化锰的混合物制取氧气.若如图中横坐标表示反应时间,纵坐标表示的是( )
在实验室加热氯酸钾和二氧化锰的混合物制取氧气.若如图中横坐标表示反应时间,纵坐标表示的是( )
 在实验室加热氯酸钾和二氧化锰的混合物制取氧气.若如图中横坐标表示反应时间,纵坐标表示的是( )
在实验室加热氯酸钾和二氧化锰的混合物制取氧气.若如图中横坐标表示反应时间,纵坐标表示的是( )| A. | 氯酸钾的质量 | B. | 钾元素的质量 | C. | 二氧化锰的质量 | D. | 生成氧气的质量 |
19.以下物品所用材料中,属于有机合成材料的是( )
| A. | 电脑塑料外壳 | B. | 真丝围巾 | C. | 不锈钢防盜门 | D. | 玻璃茶杯 |
16.某试验田的玉米叶色淡黄,有倒伏现象,你认为应该施用的复合肥是( )
| A. | CO(NH2)2 | B. | KNO3 | C. | Ca(H2PO4)2 | D. | KCl |
3.掌握科学的研究方法,探索化学世界的奥秘.
(1)分类是学习化学的重要方法之一.
①生活中,常会接触到下列物质:
A.铜丝 B.甲烷 C.过氧化氢 D.碘酒
其中属于混合物的是(填字母,下同)D,属于氧化物的是C.
②根据物质在转化过程中的特点,可将化学反应分为化合反应,分解反应、置换反应和复分解反应四种基本反应类型,下列转化不属于这四种基本反应类型的是B.
A.生石灰与水反应 B.一氧化碳还原氧化铁 C.中和反应
(2)实验是学习化学的一条重要途径,实验室中可用KClO3在MnO2催化下受热分解制取氧气,并将反应后的混合物进行分离回收,实验操作如图所示(MnO2难溶于水)

①图A中试管口略向下倾斜的原因是防止水倒流,炸裂试管,图B操作中玻璃棒的作用是搅拌,加速溶解.
②图C操作中的一处明显错误是漏斗末端没有紧靠烧杯内壁,图D操作中,当看到有较多固体析出时,停止加热.
(3)质量守恒定律是帮助我们学习的认识化学反应实质的重要理论.
①下列表述正确的是B
A.蜡烛燃烧后质量减小,说明质量守恒定律不是普遍规律
B.每32g S和32g O2完全反应后,生成64g SO2
C.在化学反应aA+bB=cC+dD中一定有:a+b=c+d
②有机化合物R与足量氧气置于密闭容器中充分反应生成CO2和H2O,实验测得反应前后物质的质量如下表:
则x=88,已知参加反应的物质R与氧气的分子个数之比为1:3,则R的相对分子质量是46.
(1)分类是学习化学的重要方法之一.
①生活中,常会接触到下列物质:
A.铜丝 B.甲烷 C.过氧化氢 D.碘酒
其中属于混合物的是(填字母,下同)D,属于氧化物的是C.
②根据物质在转化过程中的特点,可将化学反应分为化合反应,分解反应、置换反应和复分解反应四种基本反应类型,下列转化不属于这四种基本反应类型的是B.
A.生石灰与水反应 B.一氧化碳还原氧化铁 C.中和反应
(2)实验是学习化学的一条重要途径,实验室中可用KClO3在MnO2催化下受热分解制取氧气,并将反应后的混合物进行分离回收,实验操作如图所示(MnO2难溶于水)

①图A中试管口略向下倾斜的原因是防止水倒流,炸裂试管,图B操作中玻璃棒的作用是搅拌,加速溶解.
②图C操作中的一处明显错误是漏斗末端没有紧靠烧杯内壁,图D操作中,当看到有较多固体析出时,停止加热.
(3)质量守恒定律是帮助我们学习的认识化学反应实质的重要理论.
①下列表述正确的是B
A.蜡烛燃烧后质量减小,说明质量守恒定律不是普遍规律
B.每32g S和32g O2完全反应后,生成64g SO2
C.在化学反应aA+bB=cC+dD中一定有:a+b=c+d
②有机化合物R与足量氧气置于密闭容器中充分反应生成CO2和H2O,实验测得反应前后物质的质量如下表:
| R | O2 | CO2 | H2O | |
| 反应前质量/g | 46 | 128 | 0 | 0 |
| 反应后质量/g | 0 | 32 | x | 54 |
20.皮蛋是我国传统的蛋制品,深受人们喜爱,由少量NaCl、CaO和过量Na2CO3混合得到的粉末状混合物A是腌制皮蛋的配方之一.
(1)某化学兴趣小组从市场获取少量混合物A于烧杯中,缓慢加入足量的蒸馏水,边加边搅拌,静置,过滤得滤液.
①该过程发生反应的化学方程式为CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
②滤液中除含有Cl-、OH-外,还含有的阴离子是CO32-.
(2)在混合物A中加入少量ZnSO4可改善皮蛋品质,该兴趣小组获得某样品,探究在混合物A中是否添加了少量ZnSO4.
设计实验方案,完成如表表格.
限选用品与试剂:稀盐酸、pH试纸、BaC12溶液、蒸馏水、AgNO3溶液.
(1)某化学兴趣小组从市场获取少量混合物A于烧杯中,缓慢加入足量的蒸馏水,边加边搅拌,静置,过滤得滤液.
①该过程发生反应的化学方程式为CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
②滤液中除含有Cl-、OH-外,还含有的阴离子是CO32-.
(2)在混合物A中加入少量ZnSO4可改善皮蛋品质,该兴趣小组获得某样品,探究在混合物A中是否添加了少量ZnSO4.
设计实验方案,完成如表表格.
限选用品与试剂:稀盐酸、pH试纸、BaC12溶液、蒸馏水、AgNO3溶液.
| 实验操作 | 预期现象和必要结论 |
| 步骤1:取少量样品于烧杯中,缓慢加入足量蒸馏水,充分搅拌,静置,过滤 | / |
| 步骤2:取少量步骤1所得的滤液于试管中,向其中加入足量的稀盐酸,振荡,观察现象.. | 有气泡生成 |
| 步骤3:向步骤2反应后溶液中滴入少量的BaCl2溶液,观察现. | 若有白色沉淀生成,说明样品中有ZnSO4; 若无明显现象,说明样品中没有ZnSO4. |
1.2016年3月联合国秘书长潘基文任命游戏“愤怒的小鸟”为绿色荣誉大使,以鼓励年轻人应对气候变化及环境污染采取积极的行动.以下哪些行为是不提倡的( )
| A. | 出行多选择自行车和公交车 | B. | 大量使用塑料袋方便购物 | ||
| C. | 植树造林,增加城市绿地面积 | D. | 对垃圾分类,回收利用 |