题目内容
19.实验室用锌和稀硫酸反应制取质量为2.0g的氢气,需要消耗锌粒的质量是多少?同时生成硫酸锌的质量是多少?分析 根据氢气的质量可以计算锌和硫酸锌的质量.
解答 解:设需要锌的质量为x,生成硫酸锌的质量是y,
Zn+H2SO4═ZnSO4+H2↑,
65 161 2
x y 2.0g
$\frac{65}{x}=\frac{2}{2.0g}$,$\frac{161}{y}=\frac{2}{2.0g}$,
解得:x=6.5g,y=16.1g,
答:需要消耗锌粒的质量是6.5g,同时生成硫酸锌的质量是16.1g.
点评 本题主要考查学生运用化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
5.从宏观到微观、从定性到定量,体现了化学学科发展的趋势.下列从微观角度对“花气袭人知骤暖”的解释最合理的是( )
| A. | 温度越高,微粒运动速率越快 | B. | 微粒间有空隙 | ||
| C. | 微粒的体积小、质量轻 | D. | 微粒在不断运动 |
11.某兴趣小组为探究铝镁合金的组成,取16克铝镁合金样品,将60克氢氧化钠溶液平均分成三份依次加入样品中(镁与氢氧化钠溶液不反应,铝与氢氧化钠溶液反应化学方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,NaAlO2溶于水,充分反应后,过滤出固体,将其洗涤、干燥、称量,得实验数据如下:
计算:
(1)从表中数据可知第一次参加反应金属铝的质量为12克;
(2)该合金中金属镁的质量分数;
(3)所用氢氧化钠溶液溶质的质量分数.
| 所加氢氧化钠溶液的次数 | 第一次 | 第二次 | 第三次 |
| 剩余固体的质量/克 | 10.6 | 5.2 | 4.0 |
(1)从表中数据可知第一次参加反应金属铝的质量为12克;
(2)该合金中金属镁的质量分数;
(3)所用氢氧化钠溶液溶质的质量分数.
8.下列化肥属于复合肥的是( )
| A. | NH4NO3 | B. | Ca(H2PO4) 2 | C. | NH3•H2O | D. | NH4H2PO4 |
9.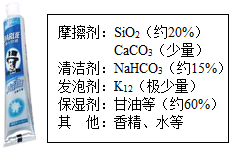 牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题.
牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题.
【已知资料】
①SiO2不溶于水,且不与酸反应.
②K12、甘油、香精等均易溶于水.
【实验探究】
Ⅰ:取一小段牙膏,加入蒸馏水,充分搅拌后静置,测得上层清液的pH为8.3,则此牙膏显碱性.
Ⅱ:兴趣小组同学设计了如下实验方案,并进行3次实验.通过测量SiO2质量,从而确定此牙膏中SiO2的质量分数.实验过程如下:
①准确称取2.0g牙膏膏体,加足量水充分溶解并过滤.
②将滤渣转移至烧杯中,加入过量稀盐酸,至看到气体不再产生为止.
③过滤、洗涤、干燥并称量得到剩余固体质量.(如表)
④据实验数据进行计算,此牙膏中SiO2的质量分数为22%.
⑤反思实验过程.
A.步骤①中加足量水的目的是使NaHCO3、K12、甘油、香精等物质充分溶解.
B.步骤②中发生反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
C.多次测量实验数据的目的是提高实验的精确度(或可信度).
D.若验证步骤②中盐酸过量,可以选择的试剂是石蕊,锌粒(至少写出类别不同的两种物质).
 牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题.
牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题.【已知资料】
①SiO2不溶于水,且不与酸反应.
②K12、甘油、香精等均易溶于水.
【实验探究】
Ⅰ:取一小段牙膏,加入蒸馏水,充分搅拌后静置,测得上层清液的pH为8.3,则此牙膏显碱性.
Ⅱ:兴趣小组同学设计了如下实验方案,并进行3次实验.通过测量SiO2质量,从而确定此牙膏中SiO2的质量分数.实验过程如下:
①准确称取2.0g牙膏膏体,加足量水充分溶解并过滤.
②将滤渣转移至烧杯中,加入过量稀盐酸,至看到气体不再产生为止.
③过滤、洗涤、干燥并称量得到剩余固体质量.(如表)
| 实验编号 | 1 | 2 | 3 |
| 实验前/g | 2.00 | 2.00 | 2.00 |
| 实验后/g | 0.43 | 0.44 | 0.45 |
⑤反思实验过程.
A.步骤①中加足量水的目的是使NaHCO3、K12、甘油、香精等物质充分溶解.
B.步骤②中发生反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
C.多次测量实验数据的目的是提高实验的精确度(或可信度).
D.若验证步骤②中盐酸过量,可以选择的试剂是石蕊,锌粒(至少写出类别不同的两种物质).