题目内容
10.下列实验基本操作中错误的是( )| A. |  | B. | 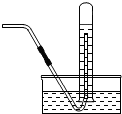 | C. | 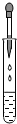 | D. | 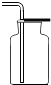 |
分析 A、根据倾倒液体的注意事项分析判断.
B、根据排水法收集气体的注意事项分析判断.
C、根据滴管的使用方法分析判断;
D、根据向上排空气法收集气体的要求进行分析判断.
解答 解:A、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨试管口,故A操作正确.
B、用排水法收集气体时,试管中装满水,倒放在装有水的水槽中,然后导管插入试管中收集气体,故B操作正确.
C、使用胶头滴管滴加少量液体时,注意胶头滴管不能伸入到试管内或接触试管内壁.应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,故C操作错误.
D、用向上排空气法收集气体时,导管一定要插入集气瓶的底部,故D操作正确.
故选C.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
5. 某校化学兴趣小组为了解碳酸氢钠粉末(NaHCO3)的化学性质,进行了如下探究.该小组成员将少量碳酸氢钠粉末置于如图装置的试管中,充分加热至反应完全,发现试管口出现无色液体,澄清石灰水变浑浊,且试管底部有白色固体残余.两位同学提出以下猜想:
某校化学兴趣小组为了解碳酸氢钠粉末(NaHCO3)的化学性质,进行了如下探究.该小组成员将少量碳酸氢钠粉末置于如图装置的试管中,充分加热至反应完全,发现试管口出现无色液体,澄清石灰水变浑浊,且试管底部有白色固体残余.两位同学提出以下猜想:
(1)提出问题:残余白色固体的成分是什么?
(2)猜想与假设:根据化学反应前后元素种类不变,两位同学提出以下猜想:
【猜想一】甲同学:“白色固体是氢氧化钠(NaOH)”;
【猜想二】乙同学:“白色固体是碳酸钠(Na2CO3)”.
(3)实验与结论:①澄清石灰水变浑浊的反应方程式:CO2+Ca(OH)2═CaCO3↓+H2O;
②为了验证自己的猜想,甲同学设计了以下方案并实验验证:
根据甲同学的猜想与验证,乙同学认为甲的结论不准确,因为NaOH与Na2CO3的水溶液均显碱性,都能使无色酚酞试液变红.
③以下是乙同学设计的实验:
④根据以上实验探究内容,写出碳酸氢钠受热分解的化学方程式:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(4)讨论交流:你还能设计不同的实验方案来验证乙同学的猜想吗?
 某校化学兴趣小组为了解碳酸氢钠粉末(NaHCO3)的化学性质,进行了如下探究.该小组成员将少量碳酸氢钠粉末置于如图装置的试管中,充分加热至反应完全,发现试管口出现无色液体,澄清石灰水变浑浊,且试管底部有白色固体残余.两位同学提出以下猜想:
某校化学兴趣小组为了解碳酸氢钠粉末(NaHCO3)的化学性质,进行了如下探究.该小组成员将少量碳酸氢钠粉末置于如图装置的试管中,充分加热至反应完全,发现试管口出现无色液体,澄清石灰水变浑浊,且试管底部有白色固体残余.两位同学提出以下猜想:(1)提出问题:残余白色固体的成分是什么?
(2)猜想与假设:根据化学反应前后元素种类不变,两位同学提出以下猜想:
【猜想一】甲同学:“白色固体是氢氧化钠(NaOH)”;
【猜想二】乙同学:“白色固体是碳酸钠(Na2CO3)”.
(3)实验与结论:①澄清石灰水变浑浊的反应方程式:CO2+Ca(OH)2═CaCO3↓+H2O;
②为了验证自己的猜想,甲同学设计了以下方案并实验验证:
| 实验步骤 | 现象 | 实验结论 |
| 取少量残余固体于试管中,加入适量的水使之溶解,往试管中滴加2滴无色酚酞溶液,观察现象 | 溶液变红 | 白色固体是氢氧化钠 |
③以下是乙同学设计的实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量残余固体于试管中, 加入适量稀盐酸,观察现象 | 试管中产生大量气泡 | 白色固体是碳酸钠 |
(4)讨论交流:你还能设计不同的实验方案来验证乙同学的猜想吗?
| 实验步骤 | 现象 | 实验结论 |
| 白色固体是碳酸钠 |
15.小冰同学在实验室中将4g由甲烷、一氧化碳和二氧化碳组成的混合气体通入足量的氧气中分别燃烧,将生成物依次通入盛有足量浓硫酸和氢氧化钠溶液的洗气瓶中,实验测得装有浓硫酸的洗气瓶增重5.4g,装有氢氧化钠的洗气瓶增重9g,则混合物中一氧化碳的质量分数为( )
| A. | 28% | B. | 35% | C. | 50% | D. | 56% |
2.小军和小明两位同学想用野外的“石头”代替大理石制取二氧化碳.他们找到一块石头(白色),为了确定其能否作代用品,请你参与他们探究白色固体成分的活动.
[查阅资料]碳酸钙在高温下分解得到氧化钙和二氧化碳.
(1)小军的探究过程是:
[作出猜想]白色固体中可能含有CaCO3.
[实验验证](写出实验步骤和现象)取试样于试管中,加入足量稀盐酸,有气泡产生.
[实验结论]猜想成立.
(2)小明的探究过程是:
[作出猜想]白色固体可能含有氧化钙.
[设计方案]
[反思与评价]小明的探究过程能证明他的猜想吗?请说明理由.不能,固体部分溶解说明还有未分解的碳酸钙
(3)根据探究,推测此石头样品的成分中含有碳酸钙和氧化钙.
[查阅资料]碳酸钙在高温下分解得到氧化钙和二氧化碳.
(1)小军的探究过程是:
[作出猜想]白色固体中可能含有CaCO3.
[实验验证](写出实验步骤和现象)取试样于试管中,加入足量稀盐酸,有气泡产生.
[实验结论]猜想成立.
(2)小明的探究过程是:
[作出猜想]白色固体可能含有氧化钙.
[设计方案]
| 操 作 | 现 象 | 结 论 |
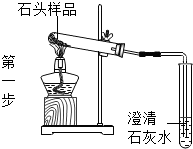 | 石头样品变疏松 | 石头样品可能发生了化学变化 |
| 澄清石灰水变浑浊 | 化学方程式为 CO2+Ca(OH)2═H20+CaCO3↓ | |
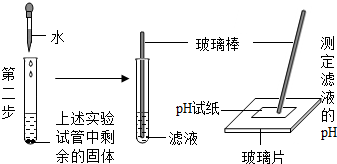 | 固体部分溶解,测得pH约为12 | 该滤液呈碱性.白色固体中含有氧化钙 |
(3)根据探究,推测此石头样品的成分中含有碳酸钙和氧化钙.
19.下列物质中的少量杂质,所选用的试剂和方法均正确的是( )
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | CO2(CO) | 足量O2 | 点燃 |
| B | CaO(CaCO3) | 少量稀盐酸 | 蒸发、结晶 |
| C | 硝酸钠溶液(硫酸钠) | 适量硝酸钡溶液 | 过滤 |
| D | CuO粉(C粉) | 适量稀盐酸 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
1.根据表中数据,回答下列问题:
(1)若要比较KNO3和NaCl在水中的溶解能力,需要控制水的质量和温度均相同.
(2)30℃时,各取4.5%KNO3固体和NaCl固体,分别加入到10g水中,充分溶解后,达到饱和状态的是NaCl溶解,该温度下,不能(选填“能”或“不能”)配制出45.8%的KNO3的溶液.
(3)根据上表提供的数据可绘制出KNO3和NaCl的溶解度曲线,两条曲线的交点所在的温度范围是B(填序号).
A.大于0℃,小于10℃B.大于20℃,小于30℃
C.大于40℃,小于50℃D.大于60℃,小于70℃
(4)将20℃时KNO3和NaCl的饱和溶液升温到80℃(不考虑水分的蒸发),溶质量分数NaCl溶液.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | |
| 溶解度/g | KNO3 | 13.3 | 20.5 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 | |
(2)30℃时,各取4.5%KNO3固体和NaCl固体,分别加入到10g水中,充分溶解后,达到饱和状态的是NaCl溶解,该温度下,不能(选填“能”或“不能”)配制出45.8%的KNO3的溶液.
(3)根据上表提供的数据可绘制出KNO3和NaCl的溶解度曲线,两条曲线的交点所在的温度范围是B(填序号).
A.大于0℃,小于10℃B.大于20℃,小于30℃
C.大于40℃,小于50℃D.大于60℃,小于70℃
(4)将20℃时KNO3和NaCl的饱和溶液升温到80℃(不考虑水分的蒸发),溶质量分数NaCl溶液.
 如图1是a、b、c三种物质的溶解度曲线,回答下列问题:
如图1是a、b、c三种物质的溶解度曲线,回答下列问题: