题目内容
18.将铁钉(a)放入潮湿的空气中易变成锈蚀的铁钉(b),把锈蚀的铁钉(b)放入适量的稀硫酸中反应后得到光亮的铁钉(c).(1)a、b、c的质量由大到小排序是b>a>c;
(2)除锈反应的化学方程式:Fe203+3H2SO4=Fe2(SO4)3+3H2O,若仅进行该反应的实验,充分反应后,观察到的现象是铁锈消失,溶液变为黄色.
分析 (1)根据铁生锈会结合氧气、氧化铁会和盐酸反应使剩下的铁质量减轻分析;
(2)根据铁锈的成分为氧化铁,与硫酸反应生成硫酸铁铁和水,铁离子为黄色,以此来解答.
解答 解:
(1)铁生锈会结合氧气生成的铁锈的质量增加,因此b>a;氧化铁会和盐酸反应是部分铁元素以氧化铁的形式溶解到溶液中了,使剩下的铁质量减轻,因此a>c;
(2)用稀硫酸除铁锈,反应的化学方程式为:Fe203+3H2SO4=Fe2(SO4)3+3H2O;除锈过程中观察到铁锈消失,溶液变为黄色.
故答案为:
(1)b>a>c.
(2)Fe203+3H2SO4=Fe2(SO4)3+3H2O;铁锈消失,溶液变为黄色.
点评 本题考查的是铁的锈蚀和除锈、铁的化学性质等方面的知识,完成此题,可以依据已有的知识进行.解答本题要求学生掌握教材中所学习的化学知识并能熟练书写化学方程式,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
相关题目
8.下列各组离子在水溶液中能大量共存的是( )
| A. | Ca2+、CO32-、OH- | B. | Na+、SO42-、OH- | C. | H+、Cl-、OH- | D. | Ag+、NH4+、Cl- |
6.以下家庭食品制作中,发生了化学变化的是( )
| A. | 剁碎花椒 | B. | 鲜榨果汁 | C. | 烘焙糕点 | D. | 凉拌黄瓜 |
13.根据如图提供的信息,下列说法中不正确的是( )


| A. | t1℃时,65 g甲的饱和溶液中含有溶剂50 g | |
| B. | 将t2℃时甲、乙、丙三种物质的饱和溶液降温至t1℃时,只有丙溶液中溶质的质量分数保持不变 | |
| C. | 在t2℃,甲、乙两种溶液中溶质的质量分数相等 | |
| D. | 乙中含少量甲时,用蒸发结晶的方法除去乙中的甲 |
10.下列实验基本操作中错误的是( )
| A. |  | B. | 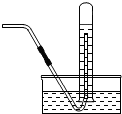 | C. | 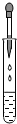 | D. | 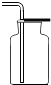 |
9.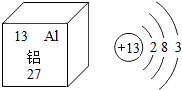 如图是有关铝元素的某些信息,下列有关铝的说法中正确的是( )
如图是有关铝元素的某些信息,下列有关铝的说法中正确的是( )
 如图是有关铝元素的某些信息,下列有关铝的说法中正确的是( )
如图是有关铝元素的某些信息,下列有关铝的说法中正确的是( )| A. | 原子核内质子数为13 | B. | 相对原子质量为27g | ||
| C. | 铝元素属于非金属元素 | D. | D、在化学变化中容易得到3个电子 |