题目内容
2.小军和小明两位同学想用野外的“石头”代替大理石制取二氧化碳.他们找到一块石头(白色),为了确定其能否作代用品,请你参与他们探究白色固体成分的活动.[查阅资料]碳酸钙在高温下分解得到氧化钙和二氧化碳.
(1)小军的探究过程是:
[作出猜想]白色固体中可能含有CaCO3.
[实验验证](写出实验步骤和现象)取试样于试管中,加入足量稀盐酸,有气泡产生.
[实验结论]猜想成立.
(2)小明的探究过程是:
[作出猜想]白色固体可能含有氧化钙.
[设计方案]
| 操 作 | 现 象 | 结 论 |
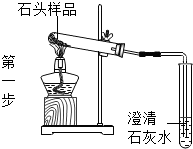 | 石头样品变疏松 | 石头样品可能发生了化学变化 |
| 澄清石灰水变浑浊 | 化学方程式为 CO2+Ca(OH)2═H20+CaCO3↓ | |
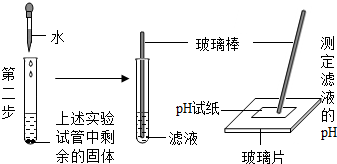 | 固体部分溶解,测得pH约为12 | 该滤液呈碱性.白色固体中含有氧化钙 |
(3)根据探究,推测此石头样品的成分中含有碳酸钙和氧化钙.
分析 [实验验证]根据检验碳酸钙可用稀盐酸来验证,因为碳酸钙与稀盐酸反应生成二氧化碳气体;
[设计方案][反思与评价]根据二氧化碳和石灰水反应产生碳酸钙沉淀和水,写出反应的方程式;
根据溶液的pH分析溶液的酸碱性,并得出结论.
解答 解:(1)白色固体可能是碳酸钙、氧化钙或二者的混合物,而小军的猜想含有碳酸钙成立,碳酸钙能够和盐酸反应产生气泡,因此可以取试样于试管中,加入足量稀盐酸,有气泡产生,说明含有碳酸钙;
(2)第一步:澄清石灰水变浑浊是石头分解产生的二氧化碳和石灰水反应产生碳酸钙沉淀和水,反应的方程式为:CO2+Ca(OH)2═H20+CaCO3↓;
第二步:因为第二步实验的现象是固体部分溶解,测得pH约为12>7,因此溶液显碱性;固体部分溶解说明还有未分解的碳酸钙,所以此石头样品的成分中含有氧化钙和碳酸钙.
(3)根据探究,推测此石头样品的成分中含有碳酸钙和氧化钙.
故答案为:(1)取试样于试管中,加入足量稀盐酸,有气泡产生;
(2)[设计方案]CO2+Ca(OH)2═H20+CaCO3↓;碱;不能,固体部分溶解说明还有未分解的碳酸钙;(3)碳酸钙和氧化钙.
点评 本题属于推断题,主要考查了碳酸钙和氧化钙的检验方法,可依据所猜想的组成物质的性质,设计实验进行猜想的验证.

练习册系列答案
相关题目
13.根据如图提供的信息,下列说法中不正确的是( )


| A. | t1℃时,65 g甲的饱和溶液中含有溶剂50 g | |
| B. | 将t2℃时甲、乙、丙三种物质的饱和溶液降温至t1℃时,只有丙溶液中溶质的质量分数保持不变 | |
| C. | 在t2℃,甲、乙两种溶液中溶质的质量分数相等 | |
| D. | 乙中含少量甲时,用蒸发结晶的方法除去乙中的甲 |
10.下列实验基本操作中错误的是( )
| A. |  | B. | 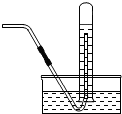 | C. | 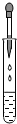 | D. | 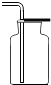 |
17.下列除去杂质的方法均正确的是( )
| 物质 | 所含杂质 | 所加药品 | 用量 | 操作 | |
| A | NaCl溶液 | NaOH和Na2CO3 | 稀盐酸 | 适量 | 加稀盐酸至恰好不再产生气泡 |
| B | CuO粉末 | C | 稀盐酸 | 足量 | 加入稀盐酸充分反应后过滤 |
| C | Cu | CuCl2固体 | 水 | 适量 | 加水搅拌后,过滤 |
| D | K2SO4 | CuSO4 | 氢氧化钾溶液 | 适量 | 加入适量氢氧化钾溶液,蒸发 |
| A. | A | B. | B | C. | C | D. | D |
13.下列叙述正确的是( )
| A. | 石油分馏可得到汽油、煤油等多种产品,属于化学变化 | |
| B. | 只有产生燃烧的化学反应才会放热 | |
| C. | 氧化反应都会放出热量 | |
| D. | 能量都是由化学反应产生的 |