题目内容
1.(1)同学们在学习氧气的化学性质时发现,可燃物的剧烈程度,除了与可燃物的性质有关,还与可燃物跟氧气的接触面积和氧气的浓度有关,某实验小组设计了一下实验,请将实验报告补充完整.| 实验 | 实验步骤 | 实验现象 | 有关反应的化学方程式 |
| A | 取得等质量的炭,分别点燃放入盛有空气和氧气集气瓶中燃烧 | 在空气中:木炭红热 在氧气中:发出明亮的白光 | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 |
| B | 取粗细不同的铁丝,分别点燃放入等体积盛有纯氧气的集气瓶中燃烧 | 粗铁丝:粗铁丝不能燃烧 细铁丝:能燃烧 | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 |
(2)在研究酸雨的危害时,进行如下探究:
【提出问题】酸雨能腐蚀自然界中的哪些物品呢?
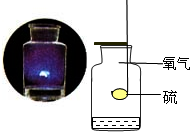
【设计实验】实验1:如图,硫在氧气中燃烧,观察到的现象是剧烈燃烧,发出明亮的蓝紫色火焰,放出大量的热,生成有刺激性气味的气体,
实验中出现的错误是集气瓶口没有加盖玻璃片.
若按正确步骤操作反应后向瓶中倒入蒸馏水,振荡,使SO2与水反应生成亚硫酸H2SO3,一段时间后,亚硫酸与氧气反应生成硫酸,有关化学反应方程式为:SO2+H2O═H2SO3;2H2SO3+O2═2H2SO4.
实验2:将所有硫酸型酸雨分成三等份,分别向其中加入如下物质,并观察到如下现象:
| 所得溶液 | 加入的物质 | 一段时间后,观察到的现象 |
| 1 | 植物树叶和果皮 | 树叶和果皮被腐蚀 |
| 2 | 镁条和铁丝 | 有气泡产生 |
| 3 | 石灰石和水泥残片 | 有气泡产生 |
【拓展与应用】怎样防治酸雨产生,请你提出两点建议:①煤进行脱硫燃烧;②减少化石燃料的使用.
分析 由氧气的化学性质,可以写出碳、铁在空气中或在氧气中燃烧的现象;由反应物、生成物及反应条件,可以写出反应的化学方程式;通过对比A、B两组实验,可从氧气的浓度、增大可燃物与氧气的接触面积等方面着手分析考虑.硫在氧气中剧烈燃烧,生成有刺激性气味的气体二氧化硫.根据反应物和生成物及其质量守恒定律可以书写化学方程式.酸雨能够腐蚀建筑物、毁坏森林树木、污染土壤和水体等.减少化石燃料的使用、工农业生产中产生的废气经过处理后再排放可以减少酸雨的形成.
解答 解:(1)碳在氧气中燃烧生成二氧化碳,细铁丝在氧气中能燃烧,生成四氧化三铁,故填:
| 实验 | 实验步骤 | 实验现象 | 有关反应的化学方程式 |
| A | 取得等质量的炭,分别点燃放入盛有空气和氧气集气瓶中燃烧 | 在空气中:木炭红热 在氧气中:发出明亮的白光 | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 |
| B | 取粗细不同的铁丝,分别点燃放入等体积盛有纯氧气的集气瓶中燃烧 | 粗铁丝:粗铁丝不能燃烧 细铁丝:能燃烧 | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 |
(2)【设计实验】硫在氧气中燃烧的实验现象为:硫在氧气中剧烈燃烧,发出明亮的蓝紫色火焰,放出大量的热,生成有刺激性气味的气体.硫燃烧生成的二氧化硫扩散到空气中会污染环境,应该在集气瓶口加上玻璃片.二氧化硫和水反应生成亚硫酸,亚硫酸和氧气反应生成硫酸,反应的化学方程式分别为:SO2+H2O═H2SO3;2H2SO3+O2═2H2SO4.故填:剧烈燃烧,发出明亮的蓝紫色火焰,放出大量的热,生成有刺激性气味的气体;集气瓶口没有加盖玻璃片;SO2+H2O═H2SO3;2H2SO3+O2═2H2SO4.
酸雨能加剧“温室效应”的依据是酸雨能和石子中的碳酸钙反应生成二氧化碳气体,故填:酸雨能和石子中的碳酸钙反应生成二氧化碳气体;
【反思与交流】酸雨能加剧“温室效应”的依据是酸雨能和石子中的碳酸钙反应生成二氧化碳气体.故填:酸雨能和石子中的碳酸钙反应生成二氧化碳气体;
【拓展与应用】煤进行脱硫燃烧、减少化石燃料的使用、工厂的废气处理后排放、开发新型能源等都可以减少酸雨的形成.故填:煤进行脱硫燃烧,减少化石燃料的使用.
点评 本题考查的是氧气的有关性质实验以及酸雨的知识,完成此题,可以依据已有的氧气的性质以及酸雨的形成和对环境的影响进行.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.测得人尿中含氮0.93%,假如这些氮都以尿素[CO(NH2)2]形式存在,则人尿中含尿素( )
| A. | 0.2% | B. | 1% | C. | 2% | D. | 3% |
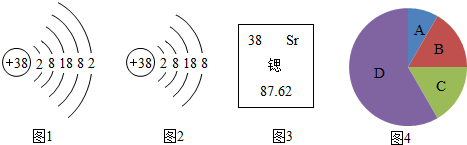
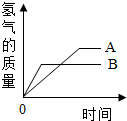 等质量的两种常见金属A和B,分别与足量的稀硫酸反应,生成正二价的金属硫酸盐和氢气.生成氢气的质量与时间关系如图,
等质量的两种常见金属A和B,分别与足量的稀硫酸反应,生成正二价的金属硫酸盐和氢气.生成氢气的质量与时间关系如图,