题目内容
12.某学校化学兴趣小组就空气中氧气的含量进行实验探究.集体讨论: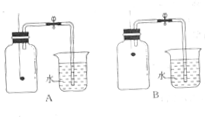
(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其他成分反应,而且生成物为固体,他们应该选择(填编号)B.
A.蜡烛 B.红磷 C.硫粉
(2)小组同学共同设计了如图所示的两套装置,你认为合理的是(填编号)A.
为了确保实验成功,在装药品之前应该检查装置的气密性.
分给实验:在讨论的基础上,他们分组进行了实验.
数据分析:实验结束后,整理数据如下:(注:集气瓶容积为100mL)
| 组 别 | 1 | 2 | 3 | 4 | 5 | 6 |
| 进入集气瓶中水的体积(mL) | 20 | 21 | 19 | 21 | 22 | 18 |
实验拓展:
(4)小组的同学作完实验后又尝试用木炭重新做了以上实验,发现水几平没有进入集气瓶.经过讨论,同学们一致认为如果事先在集气瓶内注入一些NaOH溶液来吸收二氧化碳气体,实验也能取得较好的效果.
(5)写出上述物质燃烧的文字表达式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
分析 (1)磷燃烧生成五氧化二磷固体,为保证耗尽瓶内氧气,一般加入过量的药品;
(2)同样都是红磷,放在不同的位置会对应不同的实验结果,由于氧气相对密度较大,因此让红磷在较低的位置能够更有效消耗装置内的氧气;
(3)把实验数据求平均值就是氧气的相对准确的数值,剩余气体量不变证明其难溶于水亦不能燃烧且不与红磷反应,只有氧气才能与红磷反应;
(4)木炭燃烧生成二氧化碳气体,然后根据二氧化碳的性质进行解答;
(5)根据红磷在氧气中燃烧生成五氧化二磷解答.
解答 解:(1)因为蜡烛和硫粉燃烧后产生新的气体,不能使瓶内压强改变,故选B;通常加入过量的药品,确保瓶内氧气完全消耗;故答案为:B;足量
(2)实验A和B的区别在于红磷的位置,而这一点与氧气的密度有关,由于氧气的密度大于空气,所以红磷在稍微低的位置更利于反应的进行,也更利于氧气的消耗,所以实验设计A更合理.为了确保实验的成功,在装药品之前应该 检查装置的气密性,装置漏气会使结果不准确.故答案为:A;检查装置的气密性.
(3)通过表中数据分析,平均各小组的数值为20mL,即氧气的体积为20mL,所以氧气约占空气体积的$\frac{1}{5}$;剩余气体量不变证明其难溶于水亦不能燃烧且不与红磷反应.故答案为:$\frac{1}{5}$;难溶于水、不助燃、不可燃
(4)测定空气中氧气的含量应选择能与空气中的氧气反应,并且在空气中只能与氧气反应,生成的物质只能是固体.木炭燃烧生成二氧化碳,所以应用少量的氢氧化钠溶液来吸收二氧化碳,这样就不会影响实验结果.
(5)红磷在氧气中燃烧生成五氧化二磷,反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
故答案为:
(1)B;
(2)A;检查装置的气密性.
(3)$\frac{1}{5}$;难溶于水、不助燃、不可燃
(4)NaOH溶液;
(5)4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
点评 本题主要考查用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,难度稍大.

 53随堂测系列答案
53随堂测系列答案| A. | 只含碳、氢元素 | |
| B. | 一定含碳、氧、氢三种元素 | |
| C. | 一定含有碳、氢元素,可能含有氧元素 | |
| D. | 无法确定 |
| A. | 氧元素 | B. | 氧分子 | C. | 氧原子 | D. | 氧离子 |
| A. | 食盐、碳酸钠 | B. | 酒精、浓硫酸 | C. | 碳酸钙、碳酸钠 | D. | 硫酸铜、硝酸钠 |

