题目内容
2.乙炔(C2H2)气体和氧气反应能产生高温火焰,常用于切割和焊接金属.乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时还生成一种白色固体.【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:CaO; 猜想二:CaCO3; 猜想三:Ca(OH)2.
他的依据是质量守恒定律.
【交流反思】经过同学们交流讨论,认为猜想一不成立.否定猜想一的理由是:CaO能与水反应.
【进行实验】
(一)取少量白色固体于试管中,滴加稀盐酸,没有观察到有气泡产生,证明猜想二不成立.
(二)取少量白色固体加入到水中,取上层清液,滴加无色酚酞溶液,溶液变红色,证明猜想三成立.
结论:白色固体是氢氧化钙.
写出碳化钙与水反应的化学方程式:CaC2+2H2O=Ca(OH)2+C2H2↑.
分析 【做出猜想】根据题意,乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时还生成一种白色固体,结合质量守恒定律,反应前后元素种类不变,进行分析解答.
【交流反思】根据氧化钙与水反应生成氢氧化钙,进行分析解答.
【进行实验】(一)剩余的猜想是碳酸钙和氢氧化钙,根据碳酸钙能与稀盐酸反应生成二氧化碳气体,进行分析解答.
(二)根据氢氧化钙溶液显碱性,进行分析解答.
由实验结论猜想三成立,则碳化钙(块状固体,化学式为CaC2)与水反应生成乙炔和氢氧化钙,进行分析解答.
解答 解:【做出猜想】乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时还生成一种白色固体,结合质量守恒定律,反应前后元素种类不变,白色固体是还可能是Ca(OH)2.
【交流反思】氧化钙与水反应生成氢氧化钙,故猜想一不成立.
【进行实验】(一)剩余的猜想是碳酸钙和氢氧化钙,碳酸钙能与稀盐酸反应生成二氧化碳气体,实验结论是猜想二不成立,则取少量白色固体于试管中,滴加稀盐酸,没有观察到有气泡产生.
(二)氢氧化钙溶液显碱性,取少量白色固体加入到水中,取上层清液,滴加无色酚酞溶液,溶液变红色,证明猜想三成立.
实验结论猜想三成立,则白色固体是氢氧化钙;碳化钙(块状固体,化学式为CaC2)与水反应生成乙炔和氢氧化钙,反应的化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑.
故答案为:【做出猜想】Ca(OH)2;质量守恒定律;
【交流反思】CaO能与水反应;
【进行实验】(一)有气泡产生;(二)无色酚酞溶液;
结论:氢氧化钙;CaC2+2H2O=Ca(OH)2+C2H2↑.
点评 本题难度不大,明确实验目的、熟练掌握盐与碱的化学性质、质量守恒定律、氧化钙的化学性质等是正确解答本题的关键.

练习册系列答案
相关题目
2.某工厂的废液中含有硝酸银和硝酸亚铁,某同学取适量的上述废液样品,将一定质量的镁粉加入样品中,充分反应后过滤,得到滤渣和无色滤液,下列说法不正确的是( )
| A. | 滤渣中至少含有两种金属 | |
| B. | 反应后得到滤渣的质量一定大于反应前加入的镁粉的质量 | |
| C. | 向滤渣中加入一定量稀盐酸,可能有气体生成 | |
| D. | 滤液中一定含有硝酸镁 |
11.下列物质的用途,主要利用物理性质的是( )
| A. | 氢气可用作燃料 | B. | 氮气作保护气 | ||
| C. | 稀有气体可制成电光源 | D. | 氧气用作医疗急救 |
12.某学校化学兴趣小组就空气中氧气的含量进行实验探究.集体讨论:
(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其他成分反应,而且生成物为固体,他们应该选择(填编号)B.
A.蜡烛 B.红磷 C.硫粉
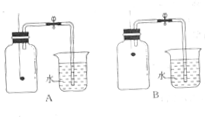
(2)小组同学共同设计了如图所示的两套装置,你认为合理的是(填编号)A.
为了确保实验成功,在装药品之前应该检查装置的气密性.
分给实验:在讨论的基础上,他们分组进行了实验.
数据分析:实验结束后,整理数据如下:(注:集气瓶容积为100mL)
(3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的$\frac{1}{5}$.通过实验还可以推断集气瓶中剩余气体的性质是难溶于水、不助燃、不可燃.(写出两条即可)
实验拓展:
(4)小组的同学作完实验后又尝试用木炭重新做了以上实验,发现水几平没有进入集气瓶.经过讨论,同学们一致认为如果事先在集气瓶内注入一些NaOH溶液来吸收二氧化碳气体,实验也能取得较好的效果.
(5)写出上述物质燃烧的文字表达式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.

(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其他成分反应,而且生成物为固体,他们应该选择(填编号)B.
A.蜡烛 B.红磷 C.硫粉
(2)小组同学共同设计了如图所示的两套装置,你认为合理的是(填编号)A.
为了确保实验成功,在装药品之前应该检查装置的气密性.
分给实验:在讨论的基础上,他们分组进行了实验.
数据分析:实验结束后,整理数据如下:(注:集气瓶容积为100mL)
| 组 别 | 1 | 2 | 3 | 4 | 5 | 6 |
| 进入集气瓶中水的体积(mL) | 20 | 21 | 19 | 21 | 22 | 18 |
实验拓展:
(4)小组的同学作完实验后又尝试用木炭重新做了以上实验,发现水几平没有进入集气瓶.经过讨论,同学们一致认为如果事先在集气瓶内注入一些NaOH溶液来吸收二氧化碳气体,实验也能取得较好的效果.
(5)写出上述物质燃烧的文字表达式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.