题目内容
12.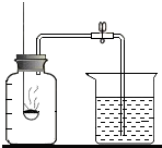 根据初中化学知识,探究空气中氧气含量实验.小明根据所学内容,红磷、白磷、木炭、镁条都可以和氧气发生反应,但是哪种物质更适用于测定空气中氧气含量,小明进行如下探究.
根据初中化学知识,探究空气中氧气含量实验.小明根据所学内容,红磷、白磷、木炭、镁条都可以和氧气发生反应,但是哪种物质更适用于测定空气中氧气含量,小明进行如下探究.【探究问题】红磷、白磷、木炭、镁条几种物质,哪种更适用于测定空气中氧气含量?
【查阅资料】
①红磷、白磷对比情况
| 红磷 | 白磷 | |
| 状态 | 暗红色固体 无毒 | 蜡状固体 有毒 |
| 燃烧温度 | 240℃ | 40℃ |
【探究过程】
如图所示,按照实验装置进行实验,探究几种物质测定空气中O2含量的可行性.
①红磷、白磷探究实验
小明认为选用红磷进行实验,其原因是红磷无毒,白磷有毒;
写出红磷与氧气燃烧的化学方程式:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
②若将实验药品改为木炭,反应结束后降至室温,打开止水夹,水不倒吸入集气瓶的原因是C和O2反应生成CO2,反应前后集气瓶内气体体积不变.
③若将实验药品改为镁条,反应结束后降至室温,观察到水倒吸入集气瓶大于$\frac{1}{5}$.根据资料信息,小明知道镁条可以与空气中的氮气、二氧化碳发生反应,进而影响反应结果.镁条与氮气反应可以生成氮化镁(Mg3N2),请写出相应的化学方程式:3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
【探究结论】几种物质中,红磷是最适用于测定空气中氧气含量.
分析 ①根据红磷和白磷的毒性选择药品;填写实验报告时根据红磷燃烧的现象和瓶内压强的改变分析,书写化学方程式要遵循质量守恒定律,注意反应条件;
②根据碳和氧气反应后生成物的状态和瓶内压强的改变分析;
③根据反应物和生成物,依据书写化学方程式的步骤完成.
解答 解:①选用红磷进行实验的原因是白磷有毒,红磷无毒;红磷燃烧产生黄色火焰,冒白烟,反应停止后冷却,打开止水夹,打开止水夹,进入集气瓶中水的体积约占 $\frac{1}{5}$,由此可得出空气中氧气约占 $\frac{1}{5}$的结论,反应的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5
②若将实验药品改为木炭,反应结束后降至室温,打开止水夹,水不倒吸入集气瓶的原因是 C和O2反应生成CO2,二氧化碳是气体,使反应前后集气瓶内气体体积不变,压强就不变,故水不能倒吸.
故答案为:C和O2反应生成CO2,反应前后集气瓶内气体体积不变.
③镁条与氮气反应可以生成氮化镁(Mg3N2);故答案为:3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;
答案:
①红磷无毒,白磷有毒;4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
②C和O2反应生成CO2,反应前后集气瓶内气体体积不变;
③3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2
点评 解决探究性实验题要过“三关”,即:审题观,要做到看清题中所讲的化学过程、看清题设条件、看清要解决的问题;分析观,想化学过程所涉及的化学概念和所用的化学原理、想所给条件与所求问题的关系、想有无隐含条件及题目考查的内容;解答观,根据题意和条件,选择最佳的答题方法,实验验证所选取的试剂要易得,操作要简单,现象要明显,结论要可靠.

| 编号 | 化学式 | C16H12N2O |
| ① | 外观 | 暗红色或深黄色片状固体 |
| ② | 溶解度 | 在水中:<0.01g/ml 汽油中:任意比例互溶 |
| ③ | 熔点 | 404-406℃ |
| ④ | 升华 | 475℃ |
| ⑤ | 致癌原因 | 在人体内分解出一种有毒的有机物(苯胺) |
(2)在上表给出的信息中,属于苏丹红物理性质的有(填编号)①、②、③、④.
(3)苏丹红1号对人体和动物都有致癌作用,主要是因为该物质在体内发生了化学变化.
【提出问题】Al2O3能不能作过氧化氢分解的催化剂呢?
【作出猜想】Al2O3能作过氧化氢分解的催化剂.
【实验验证】
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 将带火星的木条伸入装有过氧化氢溶液的试管中 | 有少量气泡 木条不复燃 | 常温下过氧化氢溶液分解速率很慢. |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中 | 产生大量的气泡 木条复燃 | Al2O3能加快过氧化氢的分解速率 |
【反思提高】经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:准确称量反应前Al2O3的质量和反应前后Al2O3的质量;
实验三的目的是Al2O3在反应前后质量是否改变.
【交流讨论】如果Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂.
【提出新的问题】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究Al2O3的化学性质在反应前后是否改变.
 福州地区的“三坊七巷”是历史文化的瑰宝,被誉为“明清古建筑博物馆”,是福州市传统文化集粹地,也是中国十大历史文化名街之一.
福州地区的“三坊七巷”是历史文化的瑰宝,被誉为“明清古建筑博物馆”,是福州市传统文化集粹地,也是中国十大历史文化名街之一. 和
和 构成的化合物Na2O.
构成的化合物Na2O.