题目内容
1.蛋氨酸(化学式为C4H11O2NS)是氨基酸中的一种.请通过计算回答下列问题:(1)蛋氨酸中各元素的质量比C:H:O:N:S=48:11:32:14:32.
(2)蛋氨酸的相对分子质量137
(3)蛋氨酸中,氮元素的质量分数是10.2% 保留到0.1%)
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(3)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
解答 解:(1)蛋氨酸中碳、氢、氧、氮、硫五种元素的质量比为(12×4):(1×11):(16×2):(14×1):(32×1)=48:11:32:14:32.
(2)蛋氨酸的相对分子质量为:12×4+1×11+16×2+14+32=137.
(3)蛋氨酸中,氮元素的质量分数是$\frac{14}{137}×$100%≈10.2%.
故答案为:(1)48:11:32:14:32;(2)149;(3)10.2%.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
12.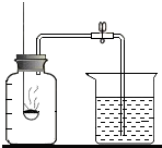 根据初中化学知识,探究空气中氧气含量实验.小明根据所学内容,红磷、白磷、木炭、镁条都可以和氧气发生反应,但是哪种物质更适用于测定空气中氧气含量,小明进行如下探究.
根据初中化学知识,探究空气中氧气含量实验.小明根据所学内容,红磷、白磷、木炭、镁条都可以和氧气发生反应,但是哪种物质更适用于测定空气中氧气含量,小明进行如下探究.
【探究问题】红磷、白磷、木炭、镁条几种物质,哪种更适用于测定空气中氧气含量?
【查阅资料】
①红磷、白磷对比情况
②镁条可以与空气中多种物质反应,如N2、CO2等
【探究过程】
如图所示,按照实验装置进行实验,探究几种物质测定空气中O2含量的可行性.
①红磷、白磷探究实验
小明认为选用红磷进行实验,其原因是红磷无毒,白磷有毒;
写出红磷与氧气燃烧的化学方程式:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
②若将实验药品改为木炭,反应结束后降至室温,打开止水夹,水不倒吸入集气瓶的原因是C和O2反应生成CO2,反应前后集气瓶内气体体积不变.
③若将实验药品改为镁条,反应结束后降至室温,观察到水倒吸入集气瓶大于$\frac{1}{5}$.根据资料信息,小明知道镁条可以与空气中的氮气、二氧化碳发生反应,进而影响反应结果.镁条与氮气反应可以生成氮化镁(Mg3N2),请写出相应的化学方程式:3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
【探究结论】几种物质中,红磷是最适用于测定空气中氧气含量.
 根据初中化学知识,探究空气中氧气含量实验.小明根据所学内容,红磷、白磷、木炭、镁条都可以和氧气发生反应,但是哪种物质更适用于测定空气中氧气含量,小明进行如下探究.
根据初中化学知识,探究空气中氧气含量实验.小明根据所学内容,红磷、白磷、木炭、镁条都可以和氧气发生反应,但是哪种物质更适用于测定空气中氧气含量,小明进行如下探究.【探究问题】红磷、白磷、木炭、镁条几种物质,哪种更适用于测定空气中氧气含量?
【查阅资料】
①红磷、白磷对比情况
| 红磷 | 白磷 | |
| 状态 | 暗红色固体 无毒 | 蜡状固体 有毒 |
| 燃烧温度 | 240℃ | 40℃ |
【探究过程】
如图所示,按照实验装置进行实验,探究几种物质测定空气中O2含量的可行性.
①红磷、白磷探究实验
小明认为选用红磷进行实验,其原因是红磷无毒,白磷有毒;
写出红磷与氧气燃烧的化学方程式:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
②若将实验药品改为木炭,反应结束后降至室温,打开止水夹,水不倒吸入集气瓶的原因是C和O2反应生成CO2,反应前后集气瓶内气体体积不变.
③若将实验药品改为镁条,反应结束后降至室温,观察到水倒吸入集气瓶大于$\frac{1}{5}$.根据资料信息,小明知道镁条可以与空气中的氮气、二氧化碳发生反应,进而影响反应结果.镁条与氮气反应可以生成氮化镁(Mg3N2),请写出相应的化学方程式:3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
【探究结论】几种物质中,红磷是最适用于测定空气中氧气含量.
 水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解有关水的一些知识.请你回答:
水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解有关水的一些知识.请你回答: 如图所示,是某同学设计的用高锰酸钾制取并收集氧气的装置图,根据图形回答有关问题:
如图所示,是某同学设计的用高锰酸钾制取并收集氧气的装置图,根据图形回答有关问题: A是某工厂废旧车床表面上红色固体的主要成分,B、C、E都是单质,D、E都没有颜色和气味,A~F是初中化学常见物质.它们之间的相互转化关系如图:
A是某工厂废旧车床表面上红色固体的主要成分,B、C、E都是单质,D、E都没有颜色和气味,A~F是初中化学常见物质.它们之间的相互转化关系如图: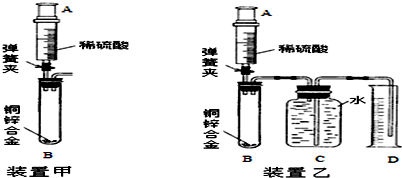
 A、B、C、D、E都是初中化学中的常见物质,相互之间存在以下转化关系.其中A是一种盐,广泛用于玻璃、造纸、纺织和洗涤的生产等;D是大理石的主要成分,大量用于建筑业.
A、B、C、D、E都是初中化学中的常见物质,相互之间存在以下转化关系.其中A是一种盐,广泛用于玻璃、造纸、纺织和洗涤的生产等;D是大理石的主要成分,大量用于建筑业.