题目内容
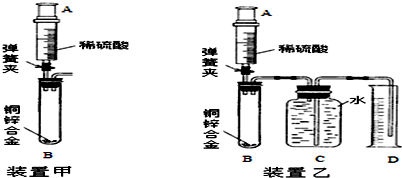
4.仔细分析下列几种情况:①红磷的量不足; ②燃烧匙插入太慢,塞紧瓶塞前空气受热逸出;③装置漏气,红磷燃烧时空气受热逸出集气瓶; ④装置漏气,冷却时空气进入集气瓶; ⑤燃烧前未将弹簧夹关闭,导致容器内气体受热膨胀从导管口逸出; ⑥未等完全冷却就观察; ⑦容器内有没反应完的氧气; ⑧导管里事先装满一部分水; ⑨用蜡烛代替红磷进行空气中氧气含量的实验探究.试回答:(1)可能导致进入瓶内水的体积明显小于瓶体积的$\frac{1}{5}$的原因有装置漏气;红磷的量不足;
(2)可能导致进入瓶内水的体积明显大于瓶体积的$\frac{1}{5}$的原因有止水夹有没有夹紧;燃烧匙伸入是否过慢等.
分析 根据红磷测定空气里氧气含量的实验原理、操作步骤、注意事项进行分析可以知道:造成测得氧气的体积分数小于五分之一的因素可以从以下四个方面考虑:(1)装置是否漏气;(2)红磷的用量是否充足;(3)瓶内的氧气是否耗尽;(4)装置是否冷却到室温;而造成测得氧气的体积分数大于五分之一的因素可以从以下两各方面考虑:(1)止水夹有没有夹紧;(2)燃烧匙伸入是否过慢等,可以根据这几个方面来分析并解答该题.
解答 解:(1)实验装置漏气,由于冷却至室温时瓶外空气进入瓶中,会导致进入水的量偏小;实验中所取红磷的量不足时,会导致装置内氧气不能全部消耗,因此使测得氧气的体积分数会小于五分之一;
(2)可能导致进入瓶内水的体积明显大于瓶体积的$\frac{1}{5}$的原因有:止水夹有没有夹紧;燃烧匙伸入是否过慢等.
故答案为:
(1)装置漏气;红磷的量不足;(2)止水夹有没有夹紧;燃烧匙伸入是否过慢等
点评 探究空气的成分,利用的原理是固态红磷燃烧消耗瓶内氧气(气体)同时生成固态物质五氧化二磷,造成瓶内气压改变,而外界气压不变,形成气压差而导致一些现象发生.

练习册系列答案
相关题目
14.学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了以下探究.
【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
(2)步骤①、②对比目的是验证检验加入氧化铜后双氧水的分解速率是否发生了变化.
(3)步骤⑦的目的是验证证明氧化铜的化学性质在反应前后没有发生改变.
【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
剧烈反应,产生大量气泡 带火星的木条复燃. | 0.2g | 溶液中有气泡放出, 带火星木条复燃 | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立. |
(3)步骤⑦的目的是验证证明氧化铜的化学性质在反应前后没有发生改变.
15.有关氧气叙述正确的是( )
| A. | 具有可燃性,用于气焊 | |
| B. | 铁丝在氧气中燃烧,火星四射 | |
| C. | 硫在氧气中燃烧,生成三氧化硫 | |
| D. | 木炭在氧气中燃烧生成有刺激性气味的气体 |
12.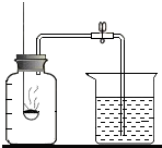 根据初中化学知识,探究空气中氧气含量实验.小明根据所学内容,红磷、白磷、木炭、镁条都可以和氧气发生反应,但是哪种物质更适用于测定空气中氧气含量,小明进行如下探究.
根据初中化学知识,探究空气中氧气含量实验.小明根据所学内容,红磷、白磷、木炭、镁条都可以和氧气发生反应,但是哪种物质更适用于测定空气中氧气含量,小明进行如下探究.
【探究问题】红磷、白磷、木炭、镁条几种物质,哪种更适用于测定空气中氧气含量?
【查阅资料】
①红磷、白磷对比情况
②镁条可以与空气中多种物质反应,如N2、CO2等
【探究过程】
如图所示,按照实验装置进行实验,探究几种物质测定空气中O2含量的可行性.
①红磷、白磷探究实验
小明认为选用红磷进行实验,其原因是红磷无毒,白磷有毒;
写出红磷与氧气燃烧的化学方程式:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
②若将实验药品改为木炭,反应结束后降至室温,打开止水夹,水不倒吸入集气瓶的原因是C和O2反应生成CO2,反应前后集气瓶内气体体积不变.
③若将实验药品改为镁条,反应结束后降至室温,观察到水倒吸入集气瓶大于$\frac{1}{5}$.根据资料信息,小明知道镁条可以与空气中的氮气、二氧化碳发生反应,进而影响反应结果.镁条与氮气反应可以生成氮化镁(Mg3N2),请写出相应的化学方程式:3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
【探究结论】几种物质中,红磷是最适用于测定空气中氧气含量.
 根据初中化学知识,探究空气中氧气含量实验.小明根据所学内容,红磷、白磷、木炭、镁条都可以和氧气发生反应,但是哪种物质更适用于测定空气中氧气含量,小明进行如下探究.
根据初中化学知识,探究空气中氧气含量实验.小明根据所学内容,红磷、白磷、木炭、镁条都可以和氧气发生反应,但是哪种物质更适用于测定空气中氧气含量,小明进行如下探究.【探究问题】红磷、白磷、木炭、镁条几种物质,哪种更适用于测定空气中氧气含量?
【查阅资料】
①红磷、白磷对比情况
| 红磷 | 白磷 | |
| 状态 | 暗红色固体 无毒 | 蜡状固体 有毒 |
| 燃烧温度 | 240℃ | 40℃ |
【探究过程】
如图所示,按照实验装置进行实验,探究几种物质测定空气中O2含量的可行性.
①红磷、白磷探究实验
小明认为选用红磷进行实验,其原因是红磷无毒,白磷有毒;
写出红磷与氧气燃烧的化学方程式:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
②若将实验药品改为木炭,反应结束后降至室温,打开止水夹,水不倒吸入集气瓶的原因是C和O2反应生成CO2,反应前后集气瓶内气体体积不变.
③若将实验药品改为镁条,反应结束后降至室温,观察到水倒吸入集气瓶大于$\frac{1}{5}$.根据资料信息,小明知道镁条可以与空气中的氮气、二氧化碳发生反应,进而影响反应结果.镁条与氮气反应可以生成氮化镁(Mg3N2),请写出相应的化学方程式:3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
【探究结论】几种物质中,红磷是最适用于测定空气中氧气含量.
5.下列叙述错误的是( )
| A. | 糖类主要为人体提供能量 | B. | 青少年常饮牛奶有利于骨骼生长 | ||
| C. | 多吃水果蔬菜可补充维生素 | D. | 六大基本营养素不含无机盐 |
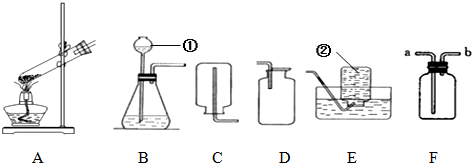
 如图所示,是某同学设计的用高锰酸钾制取并收集氧气的装置图,根据图形回答有关问题:
如图所示,是某同学设计的用高锰酸钾制取并收集氧气的装置图,根据图形回答有关问题: