题目内容
15.分析处理图表中的信息是学习化学的一种重要方法.如表是氯化钠和硝酸钾在不同温度时的溶解度,仔细阅读并回答下列问题.| 温度/℃ | 20 | 40 | 60 | 80 | |
| 溶解度/g | NaCl | 36.0 | 36.6 | 37.3 | 38.4 |
| KNO3 | 31.6 | 63.9 | 110 | 169 | |
(2)在20℃时,将40g硝酸钾固体加入到100g水中,搅拌充分后得到是饱和溶液(填“饱和”或“不饱和”)
(3)针对上述信息,甲、乙、丙三位同学分别得到如下结论,你认为说法正确的是丙.
甲:40℃时,KNO3溶液的溶质质量分数一定比NaCl溶液的溶质质量分数大.
乙:KNO3饱和溶液中一定不能再溶解NaCl固体.
丙:KNO3与NaCl溶解度相等时的温度一定在20℃-40℃之间.
分析 (1)根据表中的数据分析溶解度受温度影响较大的物质;
(2)根据在20℃时,硝酸钾的溶解度的意义分析判断;
(3)根据饱和溶液、溶解度的含义以及溶解度与溶质质量分数的关系分析判断有关的说法.
解答 解:(1)由表中的数据可知,上述两种物质中,KNO3的溶解度受温度影响较大.
(2)由表中的数据可知,在20℃时,硝酸钾的溶解度是31.6g,将40g硝酸钾固体加入到100g水中,搅拌充分后只能溶解31.6g,得到是饱和溶液.
(3)甲:溶液的状态不能确定,无法比较溶液的溶质质量分数的大小,故甲说法错误.
乙:KNO3饱和溶液中一定不能再溶解KNO3,还能溶解NaCl固体,故乙说法错误.
丙:由表中溶解度的数据可知,KNO3与NaCl溶解度相等时的温度一定在20℃-40℃之间,故丙说法正确.
故答为:(1)KNO3;(2)饱和;(3)丙.
点评 本题难度不大,掌握溶解度受温度影响的变化趋势、溶解度的含义、饱和溶液中溶质质量分数=$\frac{溶解度}{溶解度+100g}$×100%等是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5. 如图所示是甲、乙两种固体物质的溶解度曲线.下列说法中正确的是( )
如图所示是甲、乙两种固体物质的溶解度曲线.下列说法中正确的是( )
 如图所示是甲、乙两种固体物质的溶解度曲线.下列说法中正确的是( )
如图所示是甲、乙两种固体物质的溶解度曲线.下列说法中正确的是( )| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | t2℃时,向甲的饱和溶液中加入少量水,甲的溶解度变小 | |
| C. | 乙物质的饱和溶液从t2℃降到t1℃时,溶液中溶质的质量分数保持不变 | |
| D. | t2℃时,甲、乙两物质各50g,分别充分溶解于100g水中,得到的溶液质量分数相同 |
3.掌握科学的研究方法,探索化学世界的奥秘.
(1)分类是学习化学的重要方法之一.
①生活中,常会接触到下列物质:
A.铜丝 B.甲烷 C.过氧化氢 D.碘酒
其中属于混合物的是(填字母,下同)D,属于氧化物的是C.
②根据物质在转化过程中的特点,可将化学反应分为化合反应,分解反应、置换反应和复分解反应四种基本反应类型,下列转化不属于这四种基本反应类型的是B.
A.生石灰与水反应 B.一氧化碳还原氧化铁 C.中和反应
(2)实验是学习化学的一条重要途径,实验室中可用KClO3在MnO2催化下受热分解制取氧气,并将反应后的混合物进行分离回收,实验操作如图所示(MnO2难溶于水)

①图A中试管口略向下倾斜的原因是防止水倒流,炸裂试管,图B操作中玻璃棒的作用是搅拌,加速溶解.
②图C操作中的一处明显错误是漏斗末端没有紧靠烧杯内壁,图D操作中,当看到有较多固体析出时,停止加热.
(3)质量守恒定律是帮助我们学习的认识化学反应实质的重要理论.
①下列表述正确的是B
A.蜡烛燃烧后质量减小,说明质量守恒定律不是普遍规律
B.每32g S和32g O2完全反应后,生成64g SO2
C.在化学反应aA+bB=cC+dD中一定有:a+b=c+d
②有机化合物R与足量氧气置于密闭容器中充分反应生成CO2和H2O,实验测得反应前后物质的质量如下表:
则x=88,已知参加反应的物质R与氧气的分子个数之比为1:3,则R的相对分子质量是46.
(1)分类是学习化学的重要方法之一.
①生活中,常会接触到下列物质:
A.铜丝 B.甲烷 C.过氧化氢 D.碘酒
其中属于混合物的是(填字母,下同)D,属于氧化物的是C.
②根据物质在转化过程中的特点,可将化学反应分为化合反应,分解反应、置换反应和复分解反应四种基本反应类型,下列转化不属于这四种基本反应类型的是B.
A.生石灰与水反应 B.一氧化碳还原氧化铁 C.中和反应
(2)实验是学习化学的一条重要途径,实验室中可用KClO3在MnO2催化下受热分解制取氧气,并将反应后的混合物进行分离回收,实验操作如图所示(MnO2难溶于水)

①图A中试管口略向下倾斜的原因是防止水倒流,炸裂试管,图B操作中玻璃棒的作用是搅拌,加速溶解.
②图C操作中的一处明显错误是漏斗末端没有紧靠烧杯内壁,图D操作中,当看到有较多固体析出时,停止加热.
(3)质量守恒定律是帮助我们学习的认识化学反应实质的重要理论.
①下列表述正确的是B
A.蜡烛燃烧后质量减小,说明质量守恒定律不是普遍规律
B.每32g S和32g O2完全反应后,生成64g SO2
C.在化学反应aA+bB=cC+dD中一定有:a+b=c+d
②有机化合物R与足量氧气置于密闭容器中充分反应生成CO2和H2O,实验测得反应前后物质的质量如下表:
| R | O2 | CO2 | H2O | |
| 反应前质量/g | 46 | 128 | 0 | 0 |
| 反应后质量/g | 0 | 32 | x | 54 |
20.皮蛋是我国传统的蛋制品,深受人们喜爱,由少量NaCl、CaO和过量Na2CO3混合得到的粉末状混合物A是腌制皮蛋的配方之一.
(1)某化学兴趣小组从市场获取少量混合物A于烧杯中,缓慢加入足量的蒸馏水,边加边搅拌,静置,过滤得滤液.
①该过程发生反应的化学方程式为CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
②滤液中除含有Cl-、OH-外,还含有的阴离子是CO32-.
(2)在混合物A中加入少量ZnSO4可改善皮蛋品质,该兴趣小组获得某样品,探究在混合物A中是否添加了少量ZnSO4.
设计实验方案,完成如表表格.
限选用品与试剂:稀盐酸、pH试纸、BaC12溶液、蒸馏水、AgNO3溶液.
(1)某化学兴趣小组从市场获取少量混合物A于烧杯中,缓慢加入足量的蒸馏水,边加边搅拌,静置,过滤得滤液.
①该过程发生反应的化学方程式为CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
②滤液中除含有Cl-、OH-外,还含有的阴离子是CO32-.
(2)在混合物A中加入少量ZnSO4可改善皮蛋品质,该兴趣小组获得某样品,探究在混合物A中是否添加了少量ZnSO4.
设计实验方案,完成如表表格.
限选用品与试剂:稀盐酸、pH试纸、BaC12溶液、蒸馏水、AgNO3溶液.
| 实验操作 | 预期现象和必要结论 |
| 步骤1:取少量样品于烧杯中,缓慢加入足量蒸馏水,充分搅拌,静置,过滤 | / |
| 步骤2:取少量步骤1所得的滤液于试管中,向其中加入足量的稀盐酸,振荡,观察现象.. | 有气泡生成 |
| 步骤3:向步骤2反应后溶液中滴入少量的BaCl2溶液,观察现. | 若有白色沉淀生成,说明样品中有ZnSO4; 若无明显现象,说明样品中没有ZnSO4. |
7.下列叙述正确的是( )
| A. | 长期放置后不会分层的液体一定是溶液 | |
| B. | 在沉淀、吸附、过滤、消毒、蒸馏等净水过程中,消毒净化程度最高 | |
| C. | 稀释浓硫酸时,一定要把浓硫酸沿着器壁慢慢注入水里,并不断搅拌 | |
| D. | 人体摄入锌不足会引起多种疾病,所以应该大量服用补锌的保健品 |
4.下列生活中的变化过程只发生物理变化的是( )
| A. | 从铝土矿中提取金属铝 | |
| B. | 秸秆、杂草、粪便等在沼气池中发酵制得甲烷 | |
| C. | 二氧化碳气体经降温、加压制得干冰 | |
| D. | 排放到空气中的二氧化硫形成酸雨 |
5. 如图是镁元素在元素周期表的信息和原子结构示意图,下列判断不正确的是( )
如图是镁元素在元素周期表的信息和原子结构示意图,下列判断不正确的是( )
 如图是镁元素在元素周期表的信息和原子结构示意图,下列判断不正确的是( )
如图是镁元素在元素周期表的信息和原子结构示意图,下列判断不正确的是( )| A. | 一个镁原子的质量是24.31g | |
| B. | 镁原子有12个质子 | |
| C. | 镁原子在化学反应中易失去2个电子 | |
| D. | 镁元素在化合物中显正价 |
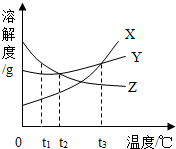 如图是X、Y、Z三种固体物质的溶解度曲线图,根据曲线图回答下列问题.
如图是X、Y、Z三种固体物质的溶解度曲线图,根据曲线图回答下列问题.