题目内容
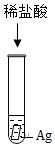
6.实验室有一瓶保管不当的试剂(如图),其残缺的标签汇总只剩下“Cl”和“5%”字样,已知它是无色液体,是初中化学常用的试剂.小强同学很感兴趣,决定对其成分进行探究:探究活动一:探究溶液的成分
提出问题:这瓶试剂可能是什么溶液呢?
老师提问:根据药品保存的位置判断,该溶液可能是稀盐酸、氯化钠溶液和氯化镁溶液中的一种.
交流讨论:根据受损标签的情况判断,这瓶试剂不可能是氯化镁,依据是氯化镁中镁离子与氯离子个数比为1﹕2,因此Cl的右下角应该有数字“2”.
设计实验并进行探究:
(1)小强为了确定该溶液是哪种溶液,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加Na2CO3溶液 | 产生大量的气泡 | 该溶液是稀盐酸,反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
探究活动二:测定溶液中溶质的质量分数
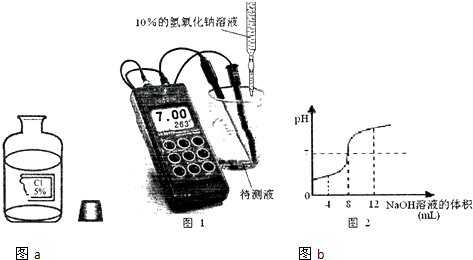
取溶液20mL于烧杯中,逐滴加入10%的氢氧化钠溶液,实验过程中用酸度计精确测定溶液的pH,从而计算溶质的质量分数,实验装置如图所示,并将该试验所测量的数据绘成图2(假设该实验温度下,待测液和NaOH溶液的密度均为1g/mL).
(2)烧杯中发生反应的化学方程式为NaOH+HCl═NaCl+H2O.
(3)当滴入NaOH溶液8mL与待测液恰好完全反应,计算出待测液中溶质的质量分数为3.65%,与标签所示的5%有偏差,造成偏差的原因是盐酸挥发,导致溶质的质量分数降低.
(4)滴入NaOH溶液12mL时,烧杯中溶液的溶质有NaOH、NaCl.
分析 探究活动一:
交流讨论:根据标签结合猜想中物质化学式的书写进行分析;
设计实验并进行探究:(1)根据碳酸钠能够和酸反应产生气体分析;
探究活动二:
(2)根据氢氧化钠和盐酸反应写出反应的方程式;
(3)根据坐标结合酸碱恰好反应的特征进行分析结合方程式进行计算,盐酸具有挥发性等分析;
(4)根据反应的产物及反应的程度分析溶质的成分.
解答 解:探究活动一:
交流讨论:因为氯化镁中镁离子与氯离子个数比为1﹕2,因此Cl的右下角应该有数字“2”,而标签Cl的右下角是1,因此不可能是氯化镁;故答案为:氯化镁;氯化镁中镁离子与氯离子个数比为1﹕2,因此Cl的右下角应该有数字“2”;
设计实验并进行探究:(1)碳酸钠能够和酸反应产生氯化钠、水和二氧化碳,反应的方程式为:Na2CO3+2HCl=NaCl+H2O+CO2↑;故答案为:稀盐酸;Na2CO3+2HCl=2NaCl+H2O+CO2↑;
探究活动二:
(2)氢氧化钠和盐酸反应,故反应的方程式为:NaOH+HCl═NaCl+H2O;故答案为:NaOH+HCl═NaCl+H2O;
(3)氢氧化钠和盐酸恰好完全反应时pH=7,因此对应的氢氧化钠是8mL;
设稀盐酸的溶质质量分数为x
NaOH+HCl═NaCl+H2O
40 36.5
8mL×1g/mL 20mL×1g/mL×x
$\frac{40}{8mL×1g/mL}$=$\frac{36.5}{20mL×1g/mL×x}$ x=3.65%;
因为盐酸易挥发,会导致溶质的质量分数降低;
故答案为:8;3.65%;盐酸挥发,导致溶质的质量分数降低;
(4)氢氧化钠和盐酸反应产生氯化钠和水,因此一定含有氯化钠;当滴入NaOH溶液12mL时,氢氧化钠过量,因此也一定含有氢氧化钠;故答案为:NaOH、NaCl.
点评 本题综合利用了物质的组成、溶液的酸碱性及物质的变化规律对未知物质进行鉴别,体现运用化学知识分析问题、解决问题的能力.

 同步奥数系列答案
同步奥数系列答案| A. | 白糖 | B. | 牛奶 | C. | 啤酒 | D. | 食醋 |
| A. | 石墨烯的化学式为C | B. | 石墨烯的硬度小于金刚石 | ||
| C. | 石墨烯属于化合物 | D. | 石墨烯不能导电 |
| A. | 用白醋长久浸泡除去铝制品水壶中的水垢 | |
| B. | 用燃烧法区分羊毛纤维和合成纤维 | |
| C. | 用活性炭吸附后过滤可将硬水转化成软水 | |
| D. | 用水扑灭电器着火 |
| A. | 一块金属很难被压缩,说明原子之间没有间隔 | |
| B. | 湿衣服晾在太阳下干的快,说明分子运动速率与温度有关 | |
| C. | 将二氧化碳气体制成干冰,体积变小是由于分子体积变小 | |
| D. | 分离液态空气制氧气说明分子可以再分 |
【提出问题1】氢氧化钠溶液变质了?
【分析】氢氧化钠溶液变质的可能原因是氢氧化钠与空气中的二氧化碳发生了化学反应.可用盐酸、氯化钡溶液试剂检验氢氧化钠溶液是否变质.
【提出问题2】该氢氧化钠溶液是全部变质还是部分变质?
【查阅资料】①已知反应:BaCl2+Na2CO3═2NaCl+BaCO3↓(白色)
②氯化钡溶液呈中性.
【设计实验】依据查阅的资料设计实验步骤,并进行实验,根据实验现象推断相应实验结论.
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量氯化钡溶液,并不断振荡. | 有白色沉淀产生. | 说明原溶液中一定含有碳酸钠. |
| (2)取(1)试管中的上层清液滴加酚酞 试液. | 溶液变红色. | 则溶液中一定含有氢氧化钠. |
| A. | 属于氧化物 | B. | 相对分子质量为154g | ||
| C. | C、H、O三种元素的质量比为10:18:1 | D. | 碳元素的质量分数最大 |
| A. | 生铁和钢有相似的化学性质--有相同原子 | |
| B. | 氧气加压后变成液氧体积减小--分子变小 | |
| C. | 酸和碱能发生中和反应--H+和OH-结合成H2O分子 | |
| D. | 氢气和液氢都可作燃料--分子相同 |