题目内容
15.蚂蚁在寻找到食物后,会分泌一种跟踪剂,其化学式为C10H18O,下列有关跟踪剂的说法正确的是( )| A. | 属于氧化物 | B. | 相对分子质量为154g | ||
| C. | C、H、O三种元素的质量比为10:18:1 | D. | 碳元素的质量分数最大 |
分析 A.氧化物是只含有两种元素且其中一种元素是氧元素的化合物,据此进行分析判断.
B.根据相对分子质量的单位来分析.
C.根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
D.根据化合物中元素质量分数大小的比较方法来分析.
解答 解:A.该信息素中含有碳、氢、氧三种元素,不属于氧化物,故错误;
B.相对分子质量的单位不是“g”而是“1”,通常省略,故错误;
C.该信息素中碳、氢、氧三种元素的质量比为(12×10):(1×18):(16×1)≠10:18:1,故错误;
D.该信息素中碳、氢、氧三种元素的质量比为(12×10):(1×18):(16×1)=60:9:8,由此可知其中碳元素的质量分数最大,故正确.
故选D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
5.植物的光合作用产生下列哪种气体( )
| A. | H2O | B. | CO2 | C. | N2 | D. | O2 |
6.实验室有一瓶保管不当的试剂(如图),其残缺的标签汇总只剩下“Cl”和“5%”字样,已知它是无色液体,是初中化学常用的试剂.小强同学很感兴趣,决定对其成分进行探究:
探究活动一:探究溶液的成分
提出问题:这瓶试剂可能是什么溶液呢?
老师提问:根据药品保存的位置判断,该溶液可能是稀盐酸、氯化钠溶液和氯化镁溶液中的一种.
交流讨论:根据受损标签的情况判断,这瓶试剂不可能是氯化镁,依据是氯化镁中镁离子与氯离子个数比为1﹕2,因此Cl的右下角应该有数字“2”.
设计实验并进行探究:
(1)小强为了确定该溶液是哪种溶液,他又进行了如下实验:
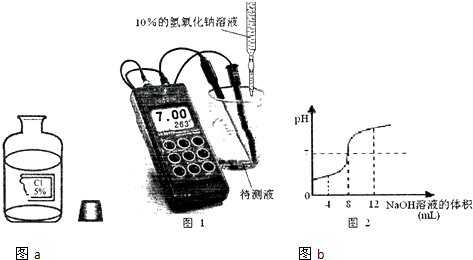
探究活动二:测定溶液中溶质的质量分数
取溶液20mL于烧杯中,逐滴加入10%的氢氧化钠溶液,实验过程中用酸度计精确测定溶液的pH,从而计算溶质的质量分数,实验装置如图所示,并将该试验所测量的数据绘成图2(假设该实验温度下,待测液和NaOH溶液的密度均为1g/mL).
(2)烧杯中发生反应的化学方程式为NaOH+HCl═NaCl+H2O.
(3)当滴入NaOH溶液8mL与待测液恰好完全反应,计算出待测液中溶质的质量分数为3.65%,与标签所示的5%有偏差,造成偏差的原因是盐酸挥发,导致溶质的质量分数降低.
(4)滴入NaOH溶液12mL时,烧杯中溶液的溶质有NaOH、NaCl.
探究活动一:探究溶液的成分
提出问题:这瓶试剂可能是什么溶液呢?
老师提问:根据药品保存的位置判断,该溶液可能是稀盐酸、氯化钠溶液和氯化镁溶液中的一种.
交流讨论:根据受损标签的情况判断,这瓶试剂不可能是氯化镁,依据是氯化镁中镁离子与氯离子个数比为1﹕2,因此Cl的右下角应该有数字“2”.
设计实验并进行探究:
(1)小强为了确定该溶液是哪种溶液,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加Na2CO3溶液 | 产生大量的气泡 | 该溶液是稀盐酸,反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑ |

探究活动二:测定溶液中溶质的质量分数
取溶液20mL于烧杯中,逐滴加入10%的氢氧化钠溶液,实验过程中用酸度计精确测定溶液的pH,从而计算溶质的质量分数,实验装置如图所示,并将该试验所测量的数据绘成图2(假设该实验温度下,待测液和NaOH溶液的密度均为1g/mL).
(2)烧杯中发生反应的化学方程式为NaOH+HCl═NaCl+H2O.
(3)当滴入NaOH溶液8mL与待测液恰好完全反应,计算出待测液中溶质的质量分数为3.65%,与标签所示的5%有偏差,造成偏差的原因是盐酸挥发,导致溶质的质量分数降低.
(4)滴入NaOH溶液12mL时,烧杯中溶液的溶质有NaOH、NaCl.
3.下列物质的用途,是利用物理性质的是( )
| A. | 氧气用于炼钢 | B. | 铜用于制作导线 | ||
| C. | 二氧化碳用作气肥 | D. | 稀有气体用作保护气 |
4.目前市场上的洁厕灵有效成分为稀盐酸,具有腐蚀性.卫生间里物品的表面不可用来清洗的是( )
| A. | 陶瓷制抽水马桶 | B. | 釉面砖(釉面主要成分是SiO2) | ||
| C. | 塑料下水管 | D. | 大理石台面(主要成分是CaCO3) |
 若取一定量的如图所示溶液配制成溶质质量分数为3%的过氧化氢溶液100g,需加入水的质量是85g.若配制时取20%的过氧化氢溶液时仰视读数,则最终配制的过氧化氢溶液的溶质质量分数偏大(填“偏大”、“偏小”或“不变”).
若取一定量的如图所示溶液配制成溶质质量分数为3%的过氧化氢溶液100g,需加入水的质量是85g.若配制时取20%的过氧化氢溶液时仰视读数,则最终配制的过氧化氢溶液的溶质质量分数偏大(填“偏大”、“偏小”或“不变”).