题目内容
1.下列有关化学在生活中的应用合力的是( )| A. | 用白醋长久浸泡除去铝制品水壶中的水垢 | |
| B. | 用燃烧法区分羊毛纤维和合成纤维 | |
| C. | 用活性炭吸附后过滤可将硬水转化成软水 | |
| D. | 用水扑灭电器着火 |
分析 A、根据白醋会与碳酸钙、氧化铝、铝等物质反应进行分析;
B、根据羊毛燃烧会产生烧焦羽毛气味的气体进行分析;
C、根据活性炭具有吸附性进行分析;
D、根据水具有导电性进行分析.
解答 解:A、白醋会与碳酸钙、氧化铝、铝等物质反应,长久浸泡会破坏表面的氧化铝薄膜,故A错误;
B、羊毛燃烧会产生烧焦羽毛气味的气体,和成纤维燃烧没有此气味,所以燃烧法可以鉴别,故B正确;
C、硬水和软水的不同是所含可溶性钙镁化合物的不同,活性炭不能将硬水软化,故C错误;
D、水具有导电性,不能用水扑灭电器着火,故D错误.
故选:B.
点评 本题难度不大,物质的性质决定物质的用途,掌握常见化学物质的性质和用途是正确解答此类题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.某同学欲测定某纯碱样品(含有氯化钠,不含不溶性杂质)中碳酸钠的质量分数,化学小组的同学设计实验,并实施实验,记录数据如下表所示:反应方程式为(Na2CO3+2HCl═2NaCl+CO2↑+H2O )
(1)求反应产生的二氧化碳的质量是4.4克.
(2)求样品中碳酸钠的质量分数.
| 空烧杯的质量 | 实验前样品和烧杯的总质量 | 加入稀盐酸的质量 | 反应后烧杯和剩余物的总质量 |
| 100.2g | 112.2g | 50g | 157.8g |
(2)求样品中碳酸钠的质量分数.
9.下列化学符号中的数字表示的意义不正确的是( )
| A. | CO2:“2”表示一个二氧化碳分子含有两个氧原子 | |
| B. | 2Fe:“2”表示两个铁元素 | |
| C. | $\stackrel{+2}{Mg}$:“+2”表示镁元素的化合价为+2价 | |
| D. | 2NH4+:“2”表示两个铵根离子 |
16.下列说法中不正确的是( )
| A. | 含铵根离子的氮肥与碱性物质混合,能产生有刺激性气味的气体 | |
| B. | 可用水来鉴定无水硫酸铜、碳酸钙、硝酸铵、氯化钠四种白色固体 | |
| C. | 将燃着的木条伸入集气瓶中,木条火焰熄灭,证明集气瓶中的气体一定是二氧化碳 | |
| D. | 检验氢氧化钠溶液中含有氯化钠的实验步骤是:先加入过量的稀硝酸,再加入硝酸银溶液 |
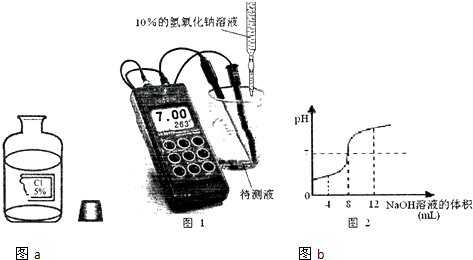
6.实验室有一瓶保管不当的试剂(如图),其残缺的标签汇总只剩下“Cl”和“5%”字样,已知它是无色液体,是初中化学常用的试剂.小强同学很感兴趣,决定对其成分进行探究:
探究活动一:探究溶液的成分
提出问题:这瓶试剂可能是什么溶液呢?
老师提问:根据药品保存的位置判断,该溶液可能是稀盐酸、氯化钠溶液和氯化镁溶液中的一种.
交流讨论:根据受损标签的情况判断,这瓶试剂不可能是氯化镁,依据是氯化镁中镁离子与氯离子个数比为1﹕2,因此Cl的右下角应该有数字“2”.
设计实验并进行探究:
(1)小强为了确定该溶液是哪种溶液,他又进行了如下实验:
探究活动二:测定溶液中溶质的质量分数
取溶液20mL于烧杯中,逐滴加入10%的氢氧化钠溶液,实验过程中用酸度计精确测定溶液的pH,从而计算溶质的质量分数,实验装置如图所示,并将该试验所测量的数据绘成图2(假设该实验温度下,待测液和NaOH溶液的密度均为1g/mL).
(2)烧杯中发生反应的化学方程式为NaOH+HCl═NaCl+H2O.
(3)当滴入NaOH溶液8mL与待测液恰好完全反应,计算出待测液中溶质的质量分数为3.65%,与标签所示的5%有偏差,造成偏差的原因是盐酸挥发,导致溶质的质量分数降低.
(4)滴入NaOH溶液12mL时,烧杯中溶液的溶质有NaOH、NaCl.
探究活动一:探究溶液的成分
提出问题:这瓶试剂可能是什么溶液呢?
老师提问:根据药品保存的位置判断,该溶液可能是稀盐酸、氯化钠溶液和氯化镁溶液中的一种.
交流讨论:根据受损标签的情况判断,这瓶试剂不可能是氯化镁,依据是氯化镁中镁离子与氯离子个数比为1﹕2,因此Cl的右下角应该有数字“2”.
设计实验并进行探究:
(1)小强为了确定该溶液是哪种溶液,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加Na2CO3溶液 | 产生大量的气泡 | 该溶液是稀盐酸,反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑ |

探究活动二:测定溶液中溶质的质量分数
取溶液20mL于烧杯中,逐滴加入10%的氢氧化钠溶液,实验过程中用酸度计精确测定溶液的pH,从而计算溶质的质量分数,实验装置如图所示,并将该试验所测量的数据绘成图2(假设该实验温度下,待测液和NaOH溶液的密度均为1g/mL).
(2)烧杯中发生反应的化学方程式为NaOH+HCl═NaCl+H2O.
(3)当滴入NaOH溶液8mL与待测液恰好完全反应,计算出待测液中溶质的质量分数为3.65%,与标签所示的5%有偏差,造成偏差的原因是盐酸挥发,导致溶质的质量分数降低.
(4)滴入NaOH溶液12mL时,烧杯中溶液的溶质有NaOH、NaCl.
13.世界上每年有上万家庭发生火灾,造成了极大损失,如果掌握一些家庭安全知识和紧急灭火措施,就能避免火灾.下列做法你认为正确的是( )
| A. | 电器着火用火扑灭 | |
| B. | 用明火检查液化气罐是否漏气 | |
| C. | 室内起火时打开门窗通风 | |
| D. | 煤气泄漏,应立即关闭阀门并开窗通风 |
 为加深对燃烧条件的认识,进一步了解灭火的原理.某同学进行了探究实验:
为加深对燃烧条件的认识,进一步了解灭火的原理.某同学进行了探究实验: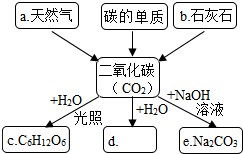 图中是某同学对二氧化碳部分知识构建的网络图,请根据图中信息用化学用语填空
图中是某同学对二氧化碳部分知识构建的网络图,请根据图中信息用化学用语填空