题目内容
7.日常生活中的下列物质,属于纯净物的是( )| A. | 白糖 | B. | 牛奶 | C. | 啤酒 | D. | 食醋 |
分析 本题考查利用纯净物的概念来判断物质是否为纯净物,宏观上看只有一种物质,微观上只有一种分子
解答 解:A、白糖是由一种物质组成,属于纯净物,故A正确;
B、牛奶中含有蛋白质、油脂等物质,属于混合物,故B错;
C、啤酒中含有水和酒精等,属于混合物,故C错;
D、食醋中含有醋酸和水等,属于混合物,故D错.
故选A.
点评 在熟悉概念的基础上能从宏观和微观两个方面来判断纯净物和混合物,还要从社会实践中了解生活中常见物质的组成.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.下列物质在氧气中燃烧,对主要现象描述正确的是( )
| A. | 硫在氧气中燃烧,产生淡蓝色火焰,放热,产生刺激性气体 | |
| B. | 一氧化碳在空气中燃烧,产生蓝色火焰,放出大量的热 | |
| C. | 向生石灰中加入水,看不到现象 | |
| D. | 将铜片插入硝酸银溶液中,开始铜片表面会覆盖一层黑色的银 |
18.地球大气的演化经历了原始大气、次生大气和现在大气三个阶段,次生大气中部分成分的微观示意图如表:
一定条件下,3.4g甲物质和4.8g氧气恰好完全反应,生成5.4g乙物质和另一种物质X,下列判断不正确的是( )
| 甲 | 乙 | 丙 |  |
 |  |  |
| A. | 物质X是氧化物 | |
| B. | 物质X的质量为2.8g | |
| C. | 物质甲的化学式是NH3 | |
| D. | 该反应化学方程式中物质X与O2的化学计量之比为2:3 |
15.生活中接触到的下列物质中,属于氧化物的是( )
| A. | 空气 | B. | 氧气 | C. | 纯碱 | D. | 干冰 |
12.除去下列物质的少量杂质(括号内为杂质),其中方法正确的是( )
| 选项 | 物质 | 除杂质方法 |
| A | CaCl2溶液(盐酸) | 加入适量的Na2CO3溶液 |
| B | NaOH溶液(Na2CO3) | 加入足量稀盐酸至不再产生气泡 |
| C | Cu(NO3)2溶液(AgNO3) | 加入过量的铜粉,过滤 |
| D | CO2(CO) | 通过足量氢氧化钙溶液,干燥 |
| A. | A | B. | B | C. | C | D. | D |
19.下列物质的类别、俗称以及化学式,说法正确的是( )
| A. | 盐-食盐-NaCl | B. | 碱-烧碱-KOH | ||
| C. | 化肥-复合肥-K2CO3 | D. | 冰-干冰-H2O |
5.植物的光合作用产生下列哪种气体( )
| A. | H2O | B. | CO2 | C. | N2 | D. | O2 |
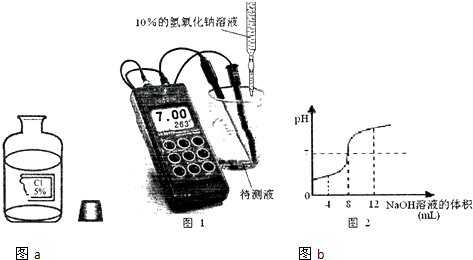
6.实验室有一瓶保管不当的试剂(如图),其残缺的标签汇总只剩下“Cl”和“5%”字样,已知它是无色液体,是初中化学常用的试剂.小强同学很感兴趣,决定对其成分进行探究:
探究活动一:探究溶液的成分
提出问题:这瓶试剂可能是什么溶液呢?
老师提问:根据药品保存的位置判断,该溶液可能是稀盐酸、氯化钠溶液和氯化镁溶液中的一种.
交流讨论:根据受损标签的情况判断,这瓶试剂不可能是氯化镁,依据是氯化镁中镁离子与氯离子个数比为1﹕2,因此Cl的右下角应该有数字“2”.
设计实验并进行探究:
(1)小强为了确定该溶液是哪种溶液,他又进行了如下实验:
探究活动二:测定溶液中溶质的质量分数
取溶液20mL于烧杯中,逐滴加入10%的氢氧化钠溶液,实验过程中用酸度计精确测定溶液的pH,从而计算溶质的质量分数,实验装置如图所示,并将该试验所测量的数据绘成图2(假设该实验温度下,待测液和NaOH溶液的密度均为1g/mL).
(2)烧杯中发生反应的化学方程式为NaOH+HCl═NaCl+H2O.
(3)当滴入NaOH溶液8mL与待测液恰好完全反应,计算出待测液中溶质的质量分数为3.65%,与标签所示的5%有偏差,造成偏差的原因是盐酸挥发,导致溶质的质量分数降低.
(4)滴入NaOH溶液12mL时,烧杯中溶液的溶质有NaOH、NaCl.
探究活动一:探究溶液的成分
提出问题:这瓶试剂可能是什么溶液呢?
老师提问:根据药品保存的位置判断,该溶液可能是稀盐酸、氯化钠溶液和氯化镁溶液中的一种.
交流讨论:根据受损标签的情况判断,这瓶试剂不可能是氯化镁,依据是氯化镁中镁离子与氯离子个数比为1﹕2,因此Cl的右下角应该有数字“2”.
设计实验并进行探究:
(1)小强为了确定该溶液是哪种溶液,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加Na2CO3溶液 | 产生大量的气泡 | 该溶液是稀盐酸,反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑ |

探究活动二:测定溶液中溶质的质量分数
取溶液20mL于烧杯中,逐滴加入10%的氢氧化钠溶液,实验过程中用酸度计精确测定溶液的pH,从而计算溶质的质量分数,实验装置如图所示,并将该试验所测量的数据绘成图2(假设该实验温度下,待测液和NaOH溶液的密度均为1g/mL).
(2)烧杯中发生反应的化学方程式为NaOH+HCl═NaCl+H2O.
(3)当滴入NaOH溶液8mL与待测液恰好完全反应,计算出待测液中溶质的质量分数为3.65%,与标签所示的5%有偏差,造成偏差的原因是盐酸挥发,导致溶质的质量分数降低.
(4)滴入NaOH溶液12mL时,烧杯中溶液的溶质有NaOH、NaCl.
 为加深对燃烧条件的认识,进一步了解灭火的原理.某同学进行了探究实验:
为加深对燃烧条件的认识,进一步了解灭火的原理.某同学进行了探究实验: