题目内容
14.下列实验设计,能达到目的是( )| A. |  探究质量守恒定律 | |
| B. |  探究Mg、Fe、Cu的金属活动性 | |
| C. | 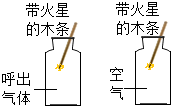 探究呼出气体和空气中氧气含量的不同 | |
| D. | 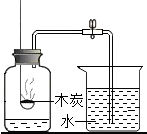 测定空气里氧气 |
分析 A、验证质量守恒若有空气中的成分常见反应或反应时有气体的产生需要在密闭的容器中进行;
B、根据金属活动顺序表中镁、铁、铜的金属活动性强弱进行解答;
C、根据呼出气体和空气都不能使带火星的木条复燃进行解答;
D、根据木条燃烧生成二氧化碳气体进行解答.
解答 解:A、锥形瓶口的单孔橡胶塞插入的是玻璃管而不是玻璃棒,白磷燃烧产生的热量及白烟会溢出装置,等装置冷却后,又会有空气的进入,应该在密闭的容器中进行,故A实验不能达到实验目的;
B、金属活动性强的金属能将金属活动性弱的金属从其盐溶液中置换出来,所以将镁条、铜分别放入氯化亚铁溶液中,镁能和氯化亚铁反应生成铁和氯化镁,而铜不能氯化亚铁反应,说明证明了三种金属的活动性顺序:镁>铁>铜;故B实验能达到实验目的;
C、呼出气体和空气都不能使带火星的木条复燃,所以不能用带火星的木条探究呼出气体和空气中氧气含量的不同,故C实验不能达到目的;
D、木炭燃烧生成二氧化碳是气体,装置内的液面无明显变化,所以不能用木条测定空气中氧气的含量,故D实验不能达到目的.
故选:B.
点评 该题主要考查对设计方案的评价,从实验的条件,现象以及可行性等方面评价.还要充分运用控制变量法的思想设计实验.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
4.在我们使用的人教版教科书设置的8个实验活动中用到研钵的是( )
| A. | 氧气的实验室制取与性质 | B. | 溶液酸碱性的检验 | ||
| C. | 粗盐中难溶性杂质的去除 | D. | 一定质量分数的氯化钠溶液的配制 |
5.如表中对部分化学知识归纳总结都正确的是( )
| A | ①热水瓶中的水垢可用食醋除去 ②洗涤剂具有乳化功能,常用来除去餐具上的油污 ③天然存在的最硬的物质是金刚石,用于镶嵌在玻璃刀头上 |
| B | ①墙内开花墙外香,说明分子在不断运动着 ②酒精溶液是混合物,说明是由不同种分子构成的 ③物质只能由分子构成 |
| C | ①用灼烧、闻气味的方法区分棉线和羊毛线 ②用观察颜色的方法区别白酒和白醋 ③用无色酚酞溶液可鉴别稀盐酸和氢氧化钠溶液 |
| D | ①霉变的大米洗净烧熟后可以食用 ②补充维生素C防止坏血病 ③利用甲醛水溶液浸泡水产品防腐 |
| A. | A | B. | B | C. | C | D. | D |
9.小明在做铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气 味,于是进行了探究.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】
(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
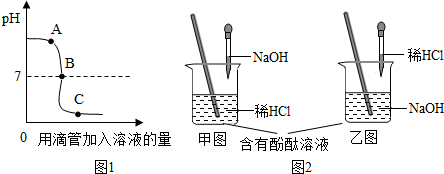
【实验探究】小明用图甲所示的装置进行实验,并将 E 中收集到的气体进行如 图乙所示的爆鸣实验.
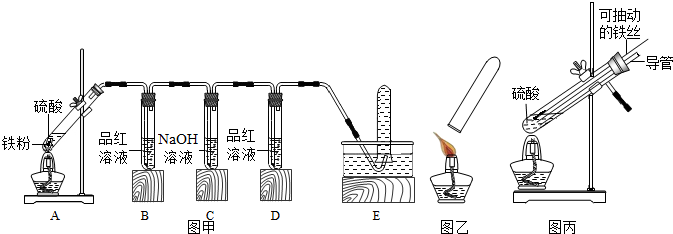
请帮助小明完成下表:
【实验结论】铁与不同浓度的硫酸溶液反应,生成的气体产物可能不同,当硫酸 浓度达到足够大时,生成的气体产物中有二氧化硫.
【交流反思】
(1)写出实验三中铁与硫酸反应的化学方程式:Fe+H2SO4═FeSO4+H2↑. 写出实验二中发生爆鸣反应的化学方程式:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
(2)实验一中 C 装置的作用是吸收二氧化硫.
【拓展延伸】小明又将 A 装置进行了如图丙所示的改进.试分析:增加的导管伸入液面以下的原因是形成液封,防止生成的气体逸出.该导管所起的作用是平衡试管内外的压强,防止停止加热时液体倒吸入试管.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】
(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】小明用图甲所示的装置进行实验,并将 E 中收集到的气体进行如 图乙所示的爆鸣实验.

请帮助小明完成下表:
| 酸浓度 | 实验现象 | A中生成气体成分 | |||
| B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
| 实验一 | 98% | 褪色 | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | 有SO2和H2 |
| 实验三 | 25% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
【交流反思】
(1)写出实验三中铁与硫酸反应的化学方程式:Fe+H2SO4═FeSO4+H2↑. 写出实验二中发生爆鸣反应的化学方程式:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
(2)实验一中 C 装置的作用是吸收二氧化硫.
【拓展延伸】小明又将 A 装置进行了如图丙所示的改进.试分析:增加的导管伸入液面以下的原因是形成液封,防止生成的气体逸出.该导管所起的作用是平衡试管内外的压强,防止停止加热时液体倒吸入试管.
19.现有MgO和Mg的混合物6.4g,将该混合物加入100g某稀硫酸中,恰好反应,把反应所得溶液蒸干,得到固体24g.下列说法正确的是( )
| A. | 生成H2的质量为0.2g | |
| B. | 该稀硫酸的溶质质量分数为9.8% | |
| C. | 反应过程中溶液的温度没有明显改变 | |
| D. | 反应前后溶液中水的质量保持不变 |
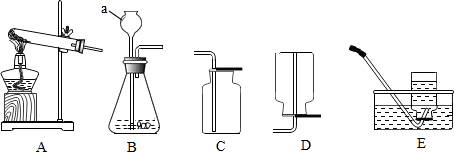
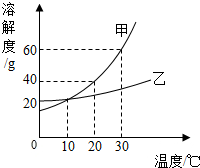 如图是甲、乙两种固体物质的溶解度曲线.据图回答:
如图是甲、乙两种固体物质的溶解度曲线.据图回答: