题目内容
1.已知下列各物质的相互转化关系如图所示,ⅹ为气体单质,C、Y中含有钠元素,D中含有氯元素.假设每次反应都恰好完全反应.
(1)写出下列物质(属溶液的写出溶质)的化学式:BCO2;ZCa(OH)2; YNaOH;CNa2CO3.
(2)写出②处发生反应的化学方程式:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
分析 根据无色气体B和澄清石灰水反应会生成碳酸钙沉淀,所以E是碳酸钙,B是二氧化碳,D中含有氯元素,碳酸钙和溶液G反应会生成二氧化碳和含有氯元素的D,所以G是盐酸,D是氯化钙,C、Y中含有钠元素,所以C是碳酸钠,Z是氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,所以Y是氢氧化钠,B和氢氧化钠反应会生成碳酸钠,所以B是二氧化碳,ⅹ为气体单质,A和X反应会生成二氧化碳,所以A可以是碳,B是氧气,然后将推出的物质进行验证即可.
解答 解:(1)无色气体B和澄清石灰水反应会生成碳酸钙沉淀,所以E是碳酸钙,B是二氧化碳,D中含有氯元素,碳酸钙和溶液G反应会生成二氧化碳和含有氯元素的D,所以G是盐酸,D是氯化钙,C、Y中含有钠元素,所以C是碳酸钠,Z是氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,所以Y是氢氧化钠,B和氢氧化钠反应会生成碳酸钠,所以B是二氧化碳,ⅹ为气体单质,A和X反应会生成二氧化碳,所以A可以是碳,B是氧气,经过验证,推导正确,所以B是CO2,Z是Ca(OH)2,Y是NaOH,C是Na2CO3;
(2)反应②是碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
故答案为:(1)CO2,Ca(OH)2,NaOH,Na2CO3;
(2)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.某化学兴趣小组探究稀盐酸与以下三种物质是否发生化学反应:
(1)甲、乙、丙三位同学设计了以下三个实验,请你填写相关内容:
(2)写出实验2的化学方程式:HCl+AgNO3 =HNO3 +AgCl↓
(3)在实验3中,因为没有明显实验现象,故无法判断该反应能否进行,为了证明该反应能否发生,甲、乙、丙三位同学又设计了如下实验方案,并继续进行实验.
【查阅资料】酸与碱发生中和反应会放出热量.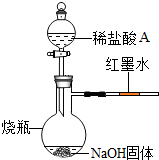
【实验设计】甲、乙、丙三位同学分别设计了如下实验方案,请你帮他们完成实验报告.
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸并不断震荡,同时测定溶液的pH,若测得溶液的pHb(填序号),则证明NaOH溶液与稀盐酸发生了化学反应.
a、逐渐增大并≥7 b、逐渐减小并≤7 c、始终不变并等于7
方案二:向NaOH溶液中滴加酚酞试液,溶液显红色,再滴加稀盐酸,若红色褪去,则证明NaOH溶液与稀盐酸发生了化学反应.
方案三:丙同学借助酸碱中和反应会放出热量,设计了如图所示的实验证明盐酸与氢氧化钠发生了反应,他观察到红墨水向右边(填“左”或“右”)移动.
【评价反思】有的同学提出,方案三的现象不足以证明NaOH与稀盐酸发生了化学反应,他的理由是:
①氢氧化钠固体溶于水会放出热量
②到底热量是氢氧化钠与盐酸反应放出的,还是氢氧化钠固体溶于水放出的,无法判断
【拓展延伸】有位同学向自己配制的氢氧化钠溶液中滴加酚酞试液时,溶液变红色,一会儿后红色消失了.①甲同学认为可能是酚酞溶液变质的缘故.你认为他的猜想是否合理?不合理(填“合理”或“不合理”)②乙同学认为可能是氢氧化钠溶液与空气中的二氧化碳反应的缘故.丙同学认为乙同学的猜想不正确,他的理由是碳酸钠呈碱性.
| K2CO3溶液 | AgNO3溶液 | NaOH溶液 |
| 实验操作 | 实验现象 | 实验结论 | |
| 实验1 | 在K2CO3溶液中加入稀盐酸 | 有气泡产生 | 稀盐酸与K2CO3溶液 发生了化学反应 |
| 实验2 | 在AgNO3溶液加入稀盐酸 | 生成白色沉淀 | 稀盐酸与在AgNO3溶液发生了化学反应 |
| 实验3 | 在NaOH溶液加入稀盐酸 | 没有现象 | 无法判断该反应能否进行 |
(3)在实验3中,因为没有明显实验现象,故无法判断该反应能否进行,为了证明该反应能否发生,甲、乙、丙三位同学又设计了如下实验方案,并继续进行实验.
【查阅资料】酸与碱发生中和反应会放出热量.

【实验设计】甲、乙、丙三位同学分别设计了如下实验方案,请你帮他们完成实验报告.
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸并不断震荡,同时测定溶液的pH,若测得溶液的pHb(填序号),则证明NaOH溶液与稀盐酸发生了化学反应.
a、逐渐增大并≥7 b、逐渐减小并≤7 c、始终不变并等于7
方案二:向NaOH溶液中滴加酚酞试液,溶液显红色,再滴加稀盐酸,若红色褪去,则证明NaOH溶液与稀盐酸发生了化学反应.
方案三:丙同学借助酸碱中和反应会放出热量,设计了如图所示的实验证明盐酸与氢氧化钠发生了反应,他观察到红墨水向右边(填“左”或“右”)移动.
【评价反思】有的同学提出,方案三的现象不足以证明NaOH与稀盐酸发生了化学反应,他的理由是:
①氢氧化钠固体溶于水会放出热量
②到底热量是氢氧化钠与盐酸反应放出的,还是氢氧化钠固体溶于水放出的,无法判断
【拓展延伸】有位同学向自己配制的氢氧化钠溶液中滴加酚酞试液时,溶液变红色,一会儿后红色消失了.①甲同学认为可能是酚酞溶液变质的缘故.你认为他的猜想是否合理?不合理(填“合理”或“不合理”)②乙同学认为可能是氢氧化钠溶液与空气中的二氧化碳反应的缘故.丙同学认为乙同学的猜想不正确,他的理由是碳酸钠呈碱性.
6.根据如图所示,下列说法错误的是( )


| A. | 装置A中,正极产生的是氧气,负极产生的是氢气 | |
| B. | 该反应产生的氢气和氧气的体积比应该是2:1 | |
| C. | 装置B中,集气瓶中放少量水是防止反应放出大量的热使集气瓶炸裂 | |
| D. | 将红热的铁丝插入盛氧气的集气瓶中时,要至上面下迅速插入 |
11.2016年3月22日是第二十届“世界水日”,3月22-28日是第二十九届“中国水周”.我国纪念2016年“世界水日”和“中国水周”活动的宣传主题为“落实五大发展理念,推进最严格水资源管理”,下列有关水的说法正确的是( )
| A. | 淡水资源取之不尽,用之不竭 | |
| B. | 过滤和加热均能使硬水转化为软水 | |
| C. | 蒸馏或用活性炭吸附可使海水转化为淡水 | |
| D. | 电解水时负极和正极生成气体的质量比为1:8 |
 从微观图判断按如图所示回答下列问题:
从微观图判断按如图所示回答下列问题: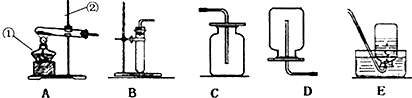
 近日,网络上出现了“不锈钢水壶中的锰会让人智力低下”等传言.对此国家食品安全专家钟凯作了解答.“不锈钢材质中的锰含量与迁移量没有任何必然联系,合金状态下,金属的惰性会增强.”钟凯指出,食品接触材料的重金属迁移量是用强酸、强碱、有机溶剂等,在较高温度下长时间浸泡模拟出来的,如果这种状态下迁移量都没问题,日常使用根本不是问题.
近日,网络上出现了“不锈钢水壶中的锰会让人智力低下”等传言.对此国家食品安全专家钟凯作了解答.“不锈钢材质中的锰含量与迁移量没有任何必然联系,合金状态下,金属的惰性会增强.”钟凯指出,食品接触材料的重金属迁移量是用强酸、强碱、有机溶剂等,在较高温度下长时间浸泡模拟出来的,如果这种状态下迁移量都没问题,日常使用根本不是问题.