题目内容
16.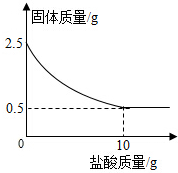 测定石灰石中的碳酸钙的含量,取出2.5克石灰石样品,逐渐加入稀盐酸,充分反应后测得剩余固体质量与加入稀盐酸的质量关系如图所示.
测定石灰石中的碳酸钙的含量,取出2.5克石灰石样品,逐渐加入稀盐酸,充分反应后测得剩余固体质量与加入稀盐酸的质量关系如图所示.(已知杂质不参与反应,也不溶于水)
(1)石灰石样品中碳酸钙的质量是2g;
(2)石灰石样品中碳酸钙的质量分数是80%;
(3)计算反应产生的气体的质量(利用化学方程式计算).
分析 碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,根据提供的信息可以进行相关方面的计算和判断.
解答 解:(1)石灰石样品中杂质质量是0.5g,碳酸钙质量是:2.5g-0.5g=2g,
故填:2g.
(2)石灰石样品中碳酸钙的质量分数为:$\frac{2g}{2.5g}$×100%=80%,
故填:80%.
(3)设生成二氧化碳质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
2g x
$\frac{100}{2g}$=$\frac{44}{x}$,
x=0.88g,
答:生成了0.88g二氧化碳.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
17.下列物品要使用热塑性塑料制造的是( )
| A. | 食品包装塑料袋 | B. | 压力锅握柄 | C. | 电木插座 | D. | 电视机外壳 |
7.向充满CO2的软塑料瓶倒入适量澄清的石灰水后,迅速拧紧软塑料瓶的瓶盖并振荡,实验现象有:( )
①澄清的石灰水变浑浊②软塑料瓶变瘪③塑料瓶内液体由紫色变红④塑料瓶内液体变得烫手.
①澄清的石灰水变浑浊②软塑料瓶变瘪③塑料瓶内液体由紫色变红④塑料瓶内液体变得烫手.
| A. | ①②③④ | B. | ②③④ | C. | ①② | D. | ①③ |
11.下列实验操作能达到实验目的是B.
| 选项 | 实验目的 | 实验操作 |
| A. | 鉴别蒸馏水 | 观察颜色 |
| B. | 比较Fe、Cu、Ag的金属活动性 | 铁丝浸入CuSO4溶液,铜丝浸入AgNO3溶液 |
| C. | 除去CO2气体中的CO | 点燃 |
| D. | 鉴别硬水和软水 | 肥皂水 |
5.如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )
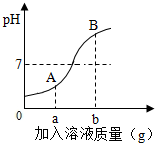

| A. | 该反应是稀HCl滴入NaOH溶液中 | |
| B. | bg是指加入氢氧化钠固体质量 | |
| C. | B点溶液的溶质为NaOH和NaCl | |
| D. | 检验B点溶液的溶质先滴加足量的MgCl2,静置后再滴入少量AgNO3 |

 .
.