题目内容
11.下列实验操作能达到实验目的是B.| 选项 | 实验目的 | 实验操作 |
| A. | 鉴别蒸馏水 | 观察颜色 |
| B. | 比较Fe、Cu、Ag的金属活动性 | 铁丝浸入CuSO4溶液,铜丝浸入AgNO3溶液 |
| C. | 除去CO2气体中的CO | 点燃 |
| D. | 鉴别硬水和软水 | 肥皂水 |
分析 蒸馏水、氯化钠溶液等都是无色的;
铁比铜活泼,铜比银活泼;
二氧化碳不能支持燃烧;
利用肥皂水可以区分硬水和软水.
解答 解:A、因为多种液体的颜色是无色的,因此不能通过观察颜色鉴别蒸馏水;
B、铁丝浸入CuSO4溶液中时,铁丝表面附着了一层红色固体,说明铁比铜活泼,铜丝浸入AgNO3溶液中时,铜丝表面附着了一层银白色固体,说明铜比银活泼,因此可以比较Fe、Cu、Ag的金属活动性;
C、二氧化碳不支持燃烧,因此不能用点燃的方法除去二氧化碳中的一氧化碳;
D、向水中加入肥皂水时,如果产生的泡沫较多,是软水,如果产生大量浮渣,是硬水,因此可以用肥皂水鉴别硬水和软水.
故选:B;
故填:肥皂水.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
12. 一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是NaOH和Na2CO3的混合物;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如表:
计算该样品中Na2CO3的质量分数.
(3)再取固体样品溶于水,加入一定质量分数的稀盐酸,直至过量.测出加入稀盐酸的质量与产生CO2气体的质量关系如图所示.从图中可以判断:在该样品溶液中加入稀盐酸,首先与之反应的物质是NaOH.
(4)请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀盐酸反应,变质前消耗盐酸的量等于变质后消耗盐酸的量(填“大于”、“小于”或“等于”).
 一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是NaOH和Na2CO3的混合物;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如表:
| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6克 | 148.5克 | 146.3克 |
(3)再取固体样品溶于水,加入一定质量分数的稀盐酸,直至过量.测出加入稀盐酸的质量与产生CO2气体的质量关系如图所示.从图中可以判断:在该样品溶液中加入稀盐酸,首先与之反应的物质是NaOH.
(4)请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀盐酸反应,变质前消耗盐酸的量等于变质后消耗盐酸的量(填“大于”、“小于”或“等于”).
19.下列烹饪用的调味品与足量水充分搅拌,不能形成溶液的是( )
| A. | 食盐 | B. | 味精 | C. | 白糖 | D. | 芝麻油 |
3.下列物质分散到足量水里能形成悬浊液的是( )
| A. | 食用油 | B. | 硝酸镁 | C. | 面粉 | D. | 氢氧化钠 |
 NaOH是化学实验中常用的试剂.
NaOH是化学实验中常用的试剂. 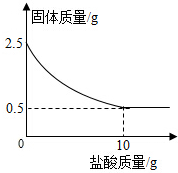 测定石灰石中的碳酸钙的含量,取出2.5克石灰石样品,逐渐加入稀盐酸,充分反应后测得剩余固体质量与加入稀盐酸的质量关系如图所示.
测定石灰石中的碳酸钙的含量,取出2.5克石灰石样品,逐渐加入稀盐酸,充分反应后测得剩余固体质量与加入稀盐酸的质量关系如图所示.
 侯德榜是我国化学工业的奠基人,纯碱工业的创始人,他发明的“侯氏制碱法”,缩短了生产流程,减少了对环境的污染,在人类化学工业史上写下了光辉的一页,侯氏制碱法的主要反应为:NH2+CO2+H2O+NaCl═NaHCO3+NH4Cl,他利用生成物中的NaHCO3溶解度较小,一经生成便会大量析出,能够很容易的分离出NaHCO3.化学小组同学模拟“侯氏制碱法”完成以下实验:10℃时,向92.6g饱和溶液中先通入足量NH3共3.4g,再通入一定量CO2至恰好完全反应,请计算:(不考虑溶解在溶液中的NH3和CO2的质量)
侯德榜是我国化学工业的奠基人,纯碱工业的创始人,他发明的“侯氏制碱法”,缩短了生产流程,减少了对环境的污染,在人类化学工业史上写下了光辉的一页,侯氏制碱法的主要反应为:NH2+CO2+H2O+NaCl═NaHCO3+NH4Cl,他利用生成物中的NaHCO3溶解度较小,一经生成便会大量析出,能够很容易的分离出NaHCO3.化学小组同学模拟“侯氏制碱法”完成以下实验:10℃时,向92.6g饱和溶液中先通入足量NH3共3.4g,再通入一定量CO2至恰好完全反应,请计算:(不考虑溶解在溶液中的NH3和CO2的质量)