题目内容
5.如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )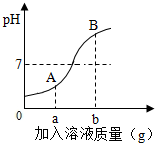
| A. | 该反应是稀HCl滴入NaOH溶液中 | |
| B. | bg是指加入氢氧化钠固体质量 | |
| C. | B点溶液的溶质为NaOH和NaCl | |
| D. | 检验B点溶液的溶质先滴加足量的MgCl2,静置后再滴入少量AgNO3 |
分析 根据图象中pH值的变化是从小于7逐渐的增大到大于7,可确定操作的过程;结合稀盐酸与氢氧化钠溶液反应生成氯化钠和水,进行分析判断.
解答 解:A、由图象可知,pH值是开始时小于7逐渐的增大到大于7,可知原溶液显酸性,然后不断的加入碱性溶液,使pH增大,说明是把氢氧化钠溶液滴加到稀盐酸中,故选项说法错误.
B、由图象可知,bg是指加入氢氧化钠溶液的质量,故选项说法错误.
C、当加入溶液的质量为bg时,溶液的pH大于7,溶液显碱性,说明氢氧化钠溶液过量,B点溶液的溶质为NaOH和NaCl,故选项说法正确.
D、B点溶液显碱性,为氢氧化钠和氯化钠的混合溶液,检验B点溶液的溶质先滴加少量的MgCl2,MgCl2与氢氧化钠溶液反应生成氢氧化镁沉淀和氯化钠,静置后再滴加少量AgNO3,由于MgCl2与氢氧化钠溶液有氯化钠生成,即使有白色沉淀生成,无法说明氯化钠是否是稀盐酸与氢氧化钠反应生成的,故选项说法错误.
故选:C.
点评 本题难度不是很大,主要考查了中和反应及其应用,掌握溶液的酸碱性和溶液pH大小之间的关系、从数形结合的角度理解中和反应是正确解答本题的关键.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
15. 向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是( )
向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是( )
 向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是( )
向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是( )| A. | a:Cl- b:K+ c:CO32- d:HCO3- | B. | a:K+b:CO32- c:Cl-d:HCO3- | ||
| C. | a:K+ b:CO32- c:HCO3- d:Cl- | D. | a:K+b:HCO3- c:Cl- d:CO32- |
13.某同学在实验室进行有关浓硫酸的实验,观察到瓶上的标签如下表所示.他从瓶中倒出100毫升用于配制稀硫酸.求:
(1)这100毫升浓硫酸的质量是多少克?
(2)若将这100毫升浓硫酸与500克水均匀混合,所得稀硫酸的质量分数是多少?(保留2位小数)
(3)欲配制1000克质量分数为19.6%的稀硫酸,需要多少毫升水?
| 浓硫酸(H2SO4)500毫升 | |
| 溶质的质量分数 | 98% |
| 密度 | 1.84克/厘米3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封储藏 | |
(2)若将这100毫升浓硫酸与500克水均匀混合,所得稀硫酸的质量分数是多少?(保留2位小数)
(3)欲配制1000克质量分数为19.6%的稀硫酸,需要多少毫升水?
10.工业生产纯碱的工艺流程示意图如下,关于如图所示4个步骤说法有错误的是( )
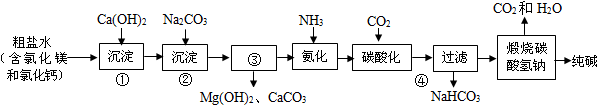

| A. | ①的目的是去除粗盐中的Mg2+ | |
| B. | ①和②这两个步骤互换不影响实验结果 | |
| C. | ③步骤为过滤 | |
| D. | 煅烧碳酸氢钠的反应属于分解反应 |
17.下列是小明课堂笔记中记录的有关化学用语,其中准确无误的是( )
| A. | 氦的元素符号:Ha | |
| B. | 2个碳酸根离子:2CO${\;}_{3}^{2-}$ | |
| C. | 氧化铝的化学式:Al2O3 | |
| D. | 镁在空气中燃烧:Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 |
15.下列化学用语与含义相符的是( )
| A. | 02---氧离子 | B. | 2H--2个氢元素 | C. | N2--2个氮原子 | D. | Hg02--氧化汞 |
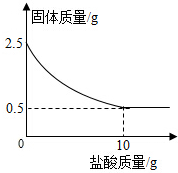 测定石灰石中的碳酸钙的含量,取出2.5克石灰石样品,逐渐加入稀盐酸,充分反应后测得剩余固体质量与加入稀盐酸的质量关系如图所示.
测定石灰石中的碳酸钙的含量,取出2.5克石灰石样品,逐渐加入稀盐酸,充分反应后测得剩余固体质量与加入稀盐酸的质量关系如图所示.
 生活中很多变化都会伴有明显的现象.
生活中很多变化都会伴有明显的现象.