题目内容
8.综合如图所示验证氢氧化钙化学性质的实验图示,回答有关问题:
(1)实验A中,一定能够观察到的明显现象是澄清的石灰水变浑浊.
(2)实验B验证了氢氧化钙能跟酸、指示剂作用.
(3)实验C中发生的反应可用化学方程式表示为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(4)已知Na2CO3溶液呈碱性,将A、B、C三个实验后的所有物质倒入同一个烧杯中,发现有气泡产生,最后只得到了无色溶液,则最后得到的无色溶液中一定含有的溶质是CaCl2、NaCl.
分析 (1)根据二氧化碳和氢氧化钙反应会生成碳酸钙沉淀和水进行分析;
(2)根据碱的性质进行分析;
(3)根据碳酸钠与氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠进行分析;
(4)根据物质间的反应来分析.
解答 解:(1)二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水,所以实验A中,一定能够观察到的明显现象是:澄清的石灰水变浑浊;
(2)氢氧化钙溶液能使无色酚酞试液变红色;
(3)碳酸钠与氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(4)碳酸钙沉淀溶解,说明碳酸钙与盐酸反应生成了氯化钙,氢氧化钠与盐酸反应生成了氯化钠,所以一定有氯化钙和氯化钠,化学式为:CaCl2、NaCl.
故答案为:(1)澄清的石灰水变浑浊;
(2)指示剂;
(3)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(4)CaCl2、NaCl.
点评 本题主要研究了由于反应物的量不同导致的生成物就不会相同的具体反应,综合性较强.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.下列化学方程式的书写及其所属基本反应类型均正确的是( )
| A. | 一氧化碳还原氧化铜:CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2置换反应 | |
| B. | 高锰酸钾分解:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$2MnO2+MnO2-O2↑分解反应 | |
| C. | 红磷在空气中燃烧:2P+5O2$\frac{\underline{\;点燃\;}}{\;}$P2O5化合反应 | |
| D. | 铝和稀硫酸反应:2Al+3H2SO4═Al2(SO4)3+3H2↑置换反应 |
16.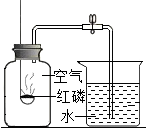 如图装置常用来测定空气中氧气的含量.下列对该实验的认识中正确的是( )
如图装置常用来测定空气中氧气的含量.下列对该实验的认识中正确的是( )
 如图装置常用来测定空气中氧气的含量.下列对该实验的认识中正确的是( )
如图装置常用来测定空气中氧气的含量.下列对该实验的认识中正确的是( )| A. | 使用红磷的量越多,最终进入集气瓶的水也越多 | |
| B. | 燃烧匙中的红磷可以换成细铁丝 | |
| C. | 该实验可说明N2难溶于水 | |
| D. | 若实验过程中,燃烧匙伸入集气瓶的速度太慢,会影响测定的结果 |
3.在一个密闭容器中放入X,Y,Z四种物质,在一定条件下发生化学反应,一段时间后,测得相关数据如下表.下列关于此反应的认识,正确的是( )
| 物质 | X | Y | Z | W |
| 反应前质量(g) | 10 | m | 8 | 7 |
| 反应后质量(g) | 2 | 3 | 30 | 25 |
| A. | 若W为水,则X或Y必定为酸或碱 | B. | 该反应可能为化合反应 | ||
| C. | m的数值为32 | D. | 参加反应的X与Y的质量比为1:4 |
20.下列物质由离子构成的是( )
| A. | 氨气 | B. | 硫酸铜 | C. | 铜 | D. | 金刚石 |
17.下列实验基本操作正确的是( )
| A. |  滴加药品 | B. | 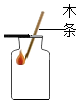 氧气验满 | C. |  液体加热 | D. | 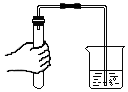 气密性检查 |
 如图中A、B、C、D、E是初中化学常见的五种不同类别的物质,E是导致温室效应的一种气体,图中“-”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略)
如图中A、B、C、D、E是初中化学常见的五种不同类别的物质,E是导致温室效应的一种气体,图中“-”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略)