题目内容
12.根据图中信息回答相关问题:
(1)请画出13号铝元素形成的离子结构示意图
 .
.(2)表中第二、三周期元素最外层电子数的变化规律是从左到右由1递增到8;其中氧、硫这两种元素的本质区别是质子数不同,它俩的化学性质相似的原因是原子的最外层电子数相同.
(3)表中最活泼的金属元素与地壳中含量最多的元素组成的化合物的化学式是Na2O.
(4)由1,6,8和11号元素组成的盐的化学式为NaHCO3.
分析 (1)根据离子结构示意图的画法来分析;
(2)根据元素周期律、元素的概念以及决定元素化学性质的因素来分析;
(3)根据化合物的化学式写法来分析;
(4)根据1、6、8和11号元素分别是H,C,O,Na组成的盐的化学式即可解答.
解答 解:(1)铝原子最外层有3个电子,在化学变化中易失去最外层电子而带上三个单位的正电荷,故填: ;
;
(2)观察表中第二、三周期各元素最外层电子数的变化可以看出最外层电子数从左到右由1递增到8.不同元素的主要区别是质子数不同,最外层电子数决定了元素的化学性质,故填:从左到右由1递增到8;质子数;最外层电子数相同;
(3)表中,钠元素最活泼,地壳中氧元素含量最高,二者组成的化合物为氧化钠,故填:Na2O;
(4)根据1、6、8和11号元素分别是H,C,O,Na组成的盐的化学式为:NaHCO3;故填:NaHCO3.
点评 本题考查学生根据元素周期表知识进行综合分析解题的能力.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
2.下列变化属于化学变化的是( )
| A. | 树变成木材 | B. | 木炭燃烧 | C. | 石蜡融化 | D. | 固体粉碎 |
6.现有20%的硫酸溶液50 克,把它配成10%的硫酸溶液,应选用的一组仪器是( )
| A. | 托盘天平、量筒、玻璃棒 | B. | 量筒、烧杯、玻璃棒 | ||
| C. | 托盘天平、量筒、烧杯 | D. | 托盘天平、烧杯、玻璃棒 |
7.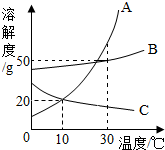 如图是A、B、C三种固体物质的溶解度曲线,下列说法不正确的是( )
如图是A、B、C三种固体物质的溶解度曲线,下列说法不正确的是( )
 如图是A、B、C三种固体物质的溶解度曲线,下列说法不正确的是( )
如图是A、B、C三种固体物质的溶解度曲线,下列说法不正确的是( )| A. | 30℃时,A、B、C三种物质的溶解度曲线由大到小的顺序是:A>B>C | |
| B. | 30℃时,A、B、C三种饱和溶液同时降温到10℃,所得溶液中溶质分数由大到小的顺序是:B>A>C | |
| C. | 10℃时,A、B、C三种饱和溶液同时升温到30℃,所得溶液中溶质分数由大到小的顺序是:B>A>C | |
| D. | 30℃时,A、B、C三种饱和溶液同时降温到10℃,析出的晶体质量大到小的顺序一定是:A>B>C |