题目内容
4.很多金属不仅能与酸反应,也能与盐溶液反应,现将a g铁钉投入到CuSO4溶液中,反应一段时间后,将固体取出洗净、烘干,称重为b g,则生成铜的质量为8(b-a)g.分析 铁比铜活泼,能和硫酸铜反应生成硫酸亚铁和铜,根据提供的数据可以计算生成铜的质量.
解答 解:设生成铜的质量为x,
Fe+CuSO4═FeSO4+Cu,固体增加的质量
56 64 64-56=8
x (b-a)g
$\frac{64}{x}$=$\frac{8}{(b-a)g}$,
x=8(b-a)g,
故填:8(b-a)g.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
14.KClO3、SO2、MnO2三种物质的组成中都含有( )
| A. | 氧分子 | B. | 氧元素 | C. | 氧气 | D. | 氧化物 |
19. 实验室有一瓶标签破损的无色溶液如图,同学们对该溶液的成分进行了探究.
实验室有一瓶标签破损的无色溶液如图,同学们对该溶液的成分进行了探究.
【提出问题】该溶液的成分是什么?
【猜想假设】①可能是CaCl2溶液;②你的猜想是Ca(OH)2溶液.
【查阅资料】CaCl2的水溶液呈中性.
【设计实验】同学们设计了如表实验方案并进行实验,请你完成实验报告.
【交流与反思】在验证猜想②的时候,小明向溶液中滴加稀盐酸,发现有少量气泡产生,可能原因是氢氧化钙与二氧化碳反应生成了碳酸钙.
 实验室有一瓶标签破损的无色溶液如图,同学们对该溶液的成分进行了探究.
实验室有一瓶标签破损的无色溶液如图,同学们对该溶液的成分进行了探究.【提出问题】该溶液的成分是什么?
【猜想假设】①可能是CaCl2溶液;②你的猜想是Ca(OH)2溶液.
【查阅资料】CaCl2的水溶液呈中性.
【设计实验】同学们设计了如表实验方案并进行实验,请你完成实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加酚酞试液 | 溶液由无色变为红色 | 猜想2成立 |
 小刚学完酸碱盐知识后设计了以下试验,仔细观察你能看到什么现象?(任答三种现象)(提示:某些非金属氧化物能和水反应生成酸,如CO2+H2O═H2CO3)
小刚学完酸碱盐知识后设计了以下试验,仔细观察你能看到什么现象?(任答三种现象)(提示:某些非金属氧化物能和水反应生成酸,如CO2+H2O═H2CO3)
 .
.
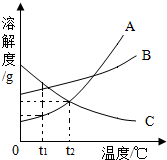 如图A、B、C为三种物质的溶解度曲线,据图回答:
如图A、B、C为三种物质的溶解度曲线,据图回答: