题目内容
12. 以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.
以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
①冷却热饱和溶液 ②蒸发溶剂 ③溶解过滤
(2)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是通入二氧化碳.
(3)40℃时的100g Na2CO3的饱和溶液中含有32.9g溶质,该溶液的溶质质量分数为32.9%.(计算结果精确到0.1)
(4)若将30%的碳酸钠溶液100g,稀释到10%,需要加水200mL.
(5)在上述(3)的配制过程中,不需要的仪器是(填序号)C.
A.托盘天平 B.100mL量筒 C.25mL量筒 D.250mL烧杯
(6)“水的蒸发”和“水的电解”两个实验中水发生变化的本质区别是(从微观视角分析)水蒸发时分子间隔变大,水电解是分子发生的变化.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)分析溶解度表可知:Na2CO3的溶解度随温度的升高而升高,且受温度影响较大;NaHCO3的溶解度随温度的升高而升高,但受温度影响变化不大.所以要出去NaHCO3固体中的少量Na2CO3,可将固体溶于水,采用蒸发结晶法,故选:②;
(2)碳酸钠、水和二氧化碳会生成碳酸钠,所以要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是通入二氧化碳,故选:C;
(3)40℃时碳酸钠的溶解度是49g,所以100gNa2CO3的饱和溶液中含有32.9g溶质,该溶液的溶质质量分数为32.9%;
(4)$\frac{100g×30%}{10%}$-100g=200g,合200mL;
(5)在上述(3)的配制过程中,不需要的仪器是25mL的量筒,故选:C;
(6))“水的蒸发”和“水的电解”两个实验中水发生变化的本质区别是:水蒸发时分子间隔变大,水电解是分子发生的变化.
故答案为:(1):②;
(2)C;
(3)32.9g,32.9%;
(4)200mL;
(5)C;
(6))水蒸发时分子间隔变大,水电解是分子发生的变化.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.小虎在做“盐酸中和氢氧化钠”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度.于是他对所得溶液的酸碱性进行了探究.
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈碱性,也可能呈中性,还可能呈酸性.
【实验验证】
【分析与思考】
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号),为避免碱性溶液污染环境,小虎对所得溶液进行了如下处理:向溶液中逐滴加入FeCl3溶液,直到不再产生沉淀为止.然后过滤,把滤液导入蒸发皿中加热,得到氯化钠晶体.
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,请你将小虎设计的实验补充完整
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈碱性,也可能呈中性,还可能呈酸性.
【实验验证】
| 实验操作 | 实验现象 | 结论 |
| 取该溶液1-2ml与试管,滴如1-2滴无色酚酞试液,震荡 | 无色酚酞试液变红 | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈中性或酸性性 |
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号),为避免碱性溶液污染环境,小虎对所得溶液进行了如下处理:向溶液中逐滴加入FeCl3溶液,直到不再产生沉淀为止.然后过滤,把滤液导入蒸发皿中加热,得到氯化钠晶体.
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,请你将小虎设计的实验补充完整
| 实验操作 | 实验现象 | 结论 |
| 取样,加入碳酸钠溶液 - | 如果有气泡产生 | 溶液呈酸性 |
| 如果没有气泡产生 | 溶液呈中性 |
2.下列除杂方案中最合理的是( )
| A. | 用点燃的方法除掉二氧化碳中混有的少量一氧化碳 | |
| B. | 加入过量的稀盐酸除掉氧化钙中的少量碳酸钙 | |
| C. | 除掉硫酸锌溶液中少量硫酸亚铁--加入过量的锌粉并过滤 | |
| D. | 除掉镁粉中少量铁粉可以加入足量的稀硫酸并过滤 |
4.下列反应不属于置换反应的是( )
| A. | 3H2+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3H2O | B. | Fe+2HCl═FeCl2+H2↑ | ||
| C. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | D. | 3Fe+4H2O$\frac{\underline{\;\;△\;\;}}{\;}$4H2+Fe3O4 |
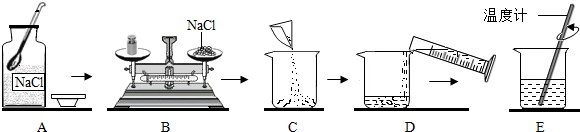
19.如图所示是实验过程中的部分操作,其中正确的是( )
| A. | 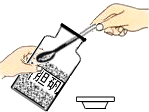 取一定量粗盐 取一定量粗盐 | B. | 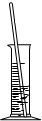 溶解 | C. | 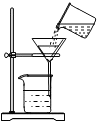 过滤 | D. |  蒸发结晶 |