题目内容
17.铁锈的主要成分的化学式Fe2O3,用稀盐酸(合理即可)除去铁锈,写出其化学方程式Fe2O3+6HCl═2FeCl3+3H2O(合理即可).分析 铁锈的主要成分是氧化铁,能与酸反应,可用稀盐酸除去铁锈,氧化铁与盐酸反应生成氯化铁和水,写出反应的化学方程式即可.
解答 解:铁锈的主要成分是氧化铁,其化学式为:Fe2O3.能与酸反应,可用稀盐酸除去铁锈,氧化铁与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O.
故答案为:Fe2O3;稀盐酸(合理即可);Fe2O3+6HCl═2FeCl3+3H2O(合理即可).
点评 本题难度不大,掌握酸的化学性质、铁锈的主要成分、化学方程式的书写方法是正确解答本题的关键.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
6.在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如表所示,下列说法错误的是( )
| 物质 | a | b | c | d |
| 反应前质(g) | 10 | 10 | 10 | 2 |
| 反应后质(g) | X | 2 | 21 | 2 |
| A. | 该反应是化合反应,d可能是催化剂 | |
| B. | a、b两种物质中元素种类一定与c物质中元素种类相同 | |
| C. | b物质可能是单质 | |
| D. | X的值为3 |
5.实验室中有一样品,已知是氧化亚铁和氧化铜组成.小科把样品均分成两份,根据学过的知识进行如下实验:
步骤一:将其中一份样品加入过量盐酸得到溶液A;
步骤二:将另一份样品在加热条件下与过量一氧化碳充分反应得到粉末B;
步骤三:将溶液A、粉末B混合,结果产生无色气体0.5克,并得到不溶于物32克和不含Cu2+的强酸性溶液.
则下列说法错误的是( )
步骤一:将其中一份样品加入过量盐酸得到溶液A;
步骤二:将另一份样品在加热条件下与过量一氧化碳充分反应得到粉末B;
步骤三:将溶液A、粉末B混合,结果产生无色气体0.5克,并得到不溶于物32克和不含Cu2+的强酸性溶液.
则下列说法错误的是( )
| A. | 溶液A的溶质中,除生成的氧化亚铁和氧化铜外,还有HCl | |
| B. | 原样品中氧化铜的质量为40g | |
| C. | 粉末B中铁的质量为28g | |
| D. | 原样品中氧化亚铁和氧化铜的质量比为9:10 |
12. 以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.
以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.
(1)要除去Na2CO3固体中的少量NaHCO3,应采用的物理方法是②(填写编号).
①冷却热饱和溶液 ②蒸发溶剂 ③溶解过滤
(2)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是通入二氧化碳.
(3)40℃时的100g Na2CO3的饱和溶液中含有32.9g溶质,该溶液的溶质质量分数为32.9%.(计算结果精确到0.1)
(4)若将30%的碳酸钠溶液100g,稀释到10%,需要加水200mL.
(5)在上述(3)的配制过程中,不需要的仪器是(填序号)C.
A.托盘天平 B.100mL量筒 C.25mL量筒 D.250mL烧杯
(6)“水的蒸发”和“水的电解”两个实验中水发生变化的本质区别是(从微观视角分析)水蒸发时分子间隔变大,水电解是分子发生的变化.
 以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.
以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
①冷却热饱和溶液 ②蒸发溶剂 ③溶解过滤
(2)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是通入二氧化碳.
(3)40℃时的100g Na2CO3的饱和溶液中含有32.9g溶质,该溶液的溶质质量分数为32.9%.(计算结果精确到0.1)
(4)若将30%的碳酸钠溶液100g,稀释到10%,需要加水200mL.
(5)在上述(3)的配制过程中,不需要的仪器是(填序号)C.
A.托盘天平 B.100mL量筒 C.25mL量筒 D.250mL烧杯
(6)“水的蒸发”和“水的电解”两个实验中水发生变化的本质区别是(从微观视角分析)水蒸发时分子间隔变大,水电解是分子发生的变化.
2.下列符号及式子中,只表示微观含义的是( )
| A. | C2H5OH | B. | H2SO4 | C. | Cu2(OH)2CO3 | D. | 3Au |
4.观察实验是学习化学的重要方法之一.以下实验现象符合事实的是( )
| A. | 测定空气中氧气含量的实验中,看到红色的铜粉逐渐变为蓝色 | |
| B. | 将镁条放入稀硫酸中,看到有大量气泡产生 | |
| C. | 在电解水实验中,正负两极产生的气体体积比约为2:1 | |
| D. | 在空气中打开盛浓盐酸的试剂瓶瓶塞,瓶口冒出白烟 |
4.下列变化中,均属于化学变化的是( )
①铁矿石被粉碎 ②铁矿石炼成生铁 ③铁制品表面刷油漆 ④铁制品生锈.
①铁矿石被粉碎 ②铁矿石炼成生铁 ③铁制品表面刷油漆 ④铁制品生锈.
| A. | ①③ | B. | ②④ | C. | ③④ | D. | ①② |
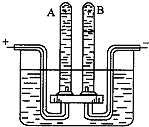 水是一种重要的自然资源,与人类和生物生存、工农业生产等息息相关.回答以下关于水的问题.
水是一种重要的自然资源,与人类和生物生存、工农业生产等息息相关.回答以下关于水的问题.