题目内容
16.下列括号中的物质是除去杂质所用药品,其中正确的是( )| A. | 氢气中有氯化氢(氢氧化钠和氧化钙固体的混合物) | |
| B. | 二氧化碳中有少量一氧化碳(氧气) | |
| C. | 氧化钙中有杂质碳酸钙(盐酸) | |
| D. | 硫酸亚铁溶液中有硫酸铜(铁粉) |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、氯化氢能与氢氧化钠反应生成氯化钠和水,氢气不与氢氧化钠和氧化钙固体反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的药品正确.
B、除去二氧化碳中的一氧化碳不能够通氧气点燃,这是因为除去气体中的气体杂质不能使用气体,否则会引入新的气体杂质,故选项所采取的药品错误.
C、氧化钙和碳酸钙均能与盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的药品错误.
D、铁粉能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的药品正确.
故选:AD.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
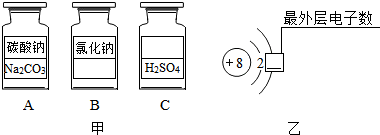
11.已知钠、钾等金属在常温下可与水发生剧烈反应,如金属钠与水反应:2Na+2H2O═2NaOH+H2↑,据此判断下列说法中不正确的是( )
| A. | 钠不能保存在水中 | |
| B. | 将石蕊溶液滴入钠与水反应后的溶液中会变成蓝色 | |
| C. | 不能用手直接拿金属钠 | |
| D. | 在此反应中,钠与参加反应的水的质量比为2:2 |
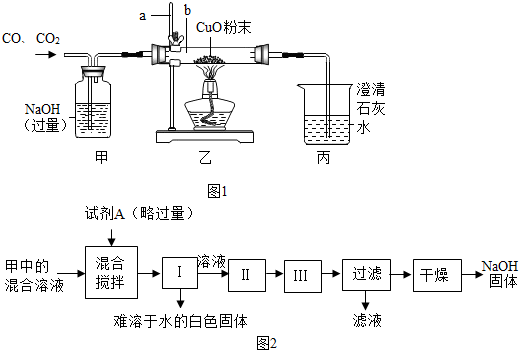
8.如图1是利用CO、CO2混合气体中的CO还原CuO的实验示意图.
①仪器a的名称是铁架台.乙装置中应该用酒精灯的外焰加热.
②写出甲中反应的化学方程式:CO2+2NaOH═Na2CO3+H2O;
乙装置的仪器b中黑色粉末变红时发生反应的化学方程式:CuO+CO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
③反应过程中,丙中可观察到的实验现象是澄清石灰水变浑浊.
④该装置存在的主要问题是缺少尾气处理装置.
⑤实验结束后,要从甲装置的混合溶液中回收得到较纯净的NaOH固体.
资料显示,在不同温度下NaOH的溶解度如下:
利用实验室的试剂和条件,实验步骤如图2(其中Ⅰ、Ⅱ、Ⅲ为实验操作):
请具体填写试剂A的化学式以及实验操作Ⅰ、Ⅲ的名称.
化学式:ACa(OH)2;
操作名称:Ⅰ过滤Ⅱ:加热蒸发形成饱和溶液Ⅲ冷却(降温结晶)
①仪器a的名称是铁架台.乙装置中应该用酒精灯的外焰加热.
②写出甲中反应的化学方程式:CO2+2NaOH═Na2CO3+H2O;
乙装置的仪器b中黑色粉末变红时发生反应的化学方程式:CuO+CO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
③反应过程中,丙中可观察到的实验现象是澄清石灰水变浑浊.
④该装置存在的主要问题是缺少尾气处理装置.
⑤实验结束后,要从甲装置的混合溶液中回收得到较纯净的NaOH固体.
资料显示,在不同温度下NaOH的溶解度如下:
| 温度(℃) | 10 | 20 | 40 | 60 | 80 | 100 |
| 溶解度(g/100g水) | 64 | 85 | 138 | 203 | 285 | 376 |
请具体填写试剂A的化学式以及实验操作Ⅰ、Ⅲ的名称.
化学式:ACa(OH)2;
操作名称:Ⅰ过滤Ⅱ:加热蒸发形成饱和溶液Ⅲ冷却(降温结晶)


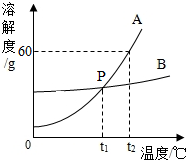 小聪同学绘制了如图A、B两种固体物质的溶解度曲线.
小聪同学绘制了如图A、B两种固体物质的溶解度曲线.