题目内容
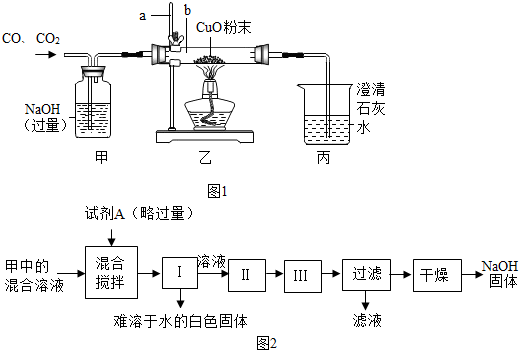
8.如图1是利用CO、CO2混合气体中的CO还原CuO的实验示意图.①仪器a的名称是铁架台.乙装置中应该用酒精灯的外焰加热.
②写出甲中反应的化学方程式:CO2+2NaOH═Na2CO3+H2O;
乙装置的仪器b中黑色粉末变红时发生反应的化学方程式:CuO+CO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
③反应过程中,丙中可观察到的实验现象是澄清石灰水变浑浊.
④该装置存在的主要问题是缺少尾气处理装置.
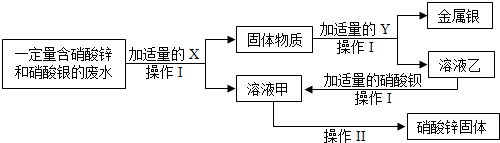
⑤实验结束后,要从甲装置的混合溶液中回收得到较纯净的NaOH固体.
资料显示,在不同温度下NaOH的溶解度如下:
| 温度(℃) | 10 | 20 | 40 | 60 | 80 | 100 |
| 溶解度(g/100g水) | 64 | 85 | 138 | 203 | 285 | 376 |
请具体填写试剂A的化学式以及实验操作Ⅰ、Ⅲ的名称.
化学式:ACa(OH)2;
操作名称:Ⅰ过滤Ⅱ:加热蒸发形成饱和溶液Ⅲ冷却(降温结晶)
分析 ①从仪器的图及用途去分析;
②二氧化碳与碱反应生成盐和水,一氧化碳还原氧化铜,生成红色铜单质和二氧化碳;
③二氧化碳与石灰水反应生成碳酸钙沉淀,使石灰水变浑浊;
④装置中缺少对尾气一氧化碳的处理;
⑤回收甲装置中的NaOH固体,实际就是先除去其中的Na2CO3杂质,再结晶出NaOH,由资料所示不同温度下NaOH的溶解度可见,其溶解度受温度影响较大,故可采用加热后降温结晶.
解答 解:①由仪器的图及用途可知仪器为:铁架台;由于酒精灯的外焰温度最高,所以乙装置中应该用酒精灯的外焰加热;故答案为:铁架台;外;
②二氧化碳与碱反应生成盐和水,一氧化碳不参与反应,一氧化碳还原氧化铜,生成红色铜单质和二氧化碳,
故填:CO2+2NaOH═Na2CO3+H2O;CuO+CO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
③二氧化碳与石灰水反应生成碳酸钙沉淀,使石灰水变浑浊,
故答案为:澄清石灰水变浑浊;
④一氧化碳有毒,不溶于水,可燃,装置中缺少对尾气一氧化碳的处理,
故答案为:缺少尾气处理装置;
⑤要从甲装置的混合溶液中回收得到较纯净的NaOH固体,要先除去其中的Na2CO3杂质,用Ca(OH)2与Na2CO3反应生成沉淀碳酸钙和氢氧化钠,过滤出沉淀,得到氢氧化钠溶液,由资料可得出氢氧化钠的溶解度受温度影响较大,可加热后再降温结晶,故答案为:Ca(OH)2;过滤;冷却(降温结晶).
点评 本题考查了一氧化碳还原氧化铜、二氧化碳与碱反应以及混合物分离除杂,前几题比较基础常见,而最后一题对学生的解题能力要求较高.

练习册系列答案
相关题目
3.下列化学反应中不属于复分解反应的是( )
| A. | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | B. | Fe2O3+6HCl=2FeCl3+3H2O | ||
| C. | Ca(OH)2+H2SO4=CaSO4+2H2O | D. | CaCO3+2HCl=CaCl2+H2O+CO2↑ |
19.为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了下列实验(已知锌的颗粒大小相同,稀盐酸的温度均为室温).下列说法正确的是( )
| 实验① | 实验② | 实验③ |
 |  |  |
| A. | 对比实验①和②,可研究盐酸的浓度对反应剧烈程度的影响 | |
| B. | 对比实验①和②,可研究温度对反应剧烈程度的影响 | |
| C. | 对比实验②和③,可研究温度对反应剧烈程度的影响 | |
| D. | 对比实验①和③,可研究盐酸的浓度对反应剧烈程度的影响 |
16.下列括号中的物质是除去杂质所用药品,其中正确的是( )
| A. | 氢气中有氯化氢(氢氧化钠和氧化钙固体的混合物) | |
| B. | 二氧化碳中有少量一氧化碳(氧气) | |
| C. | 氧化钙中有杂质碳酸钙(盐酸) | |
| D. | 硫酸亚铁溶液中有硫酸铜(铁粉) |