题目内容
5.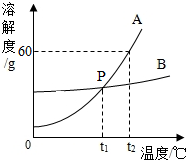 小聪同学绘制了如图A、B两种固体物质的溶解度曲线.
小聪同学绘制了如图A、B两种固体物质的溶解度曲线.(1)A物质在温度为t2℃时的溶解度是60g;t2℃时A的饱和溶液的溶质质量分数是37.5%.
(2)溶解度受温度影响变化较小的物质B,要从它的饱和溶液中大量析出晶体,宜采用蒸发方法结晶.
(3)NaCl是食盐的主要成分,Na2CO3俗称纯碱,它们都是生活和生产中的重要物质或原料.我国有许多盐碱湖,湖中溶有大量的NaCl和Na2CO3,那里的人们冬天捞碱,夏天晒盐.据此你认为上图中物质A(填“A”或“B”)的溶解度曲线与纯碱的溶解度曲线相似.
分析 (1)根据物质的溶解度曲线可以判断物质在某一温度时的溶解度;
饱和溶液中溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%;
(2)从溶液中结晶的方法有两种:蒸发结晶和降温结晶,物质的溶解度受温度变化影响较小时,应该用蒸发结晶;物质的溶解度受温度变化影响较大时,应该用降温结晶;
(3)冬天捞碱,说明碳酸钠的溶解度随着温度的升高而增大,并且受温度变化影响较大;
夏天晒盐,说明氯化钠的溶解度受温度影响较小.
解答 解:(1)由物质的溶解度曲线可知,A物质在温度为t2℃时的溶解度是60g;
t2℃时A的饱和溶液的溶质质量分数=$\frac{60g}{100g+60g}$×100%=37.5%.
故填:60g;37.5%.
(2)溶解度受温度影响变化较小的物质B,要从它的饱和溶液中大量析出晶体,宜采用蒸发的方法结晶.
故填:蒸发.
(3)人们冬天捞碱,夏天晒盐,说明碳酸钠的溶解度受温度饱和影响较大,氯化钠的溶解度受温度饱和影响较小,因此A的溶解度曲线与纯碱的溶解度曲线相似.
故填:A.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
相关题目
16.下列括号中的物质是除去杂质所用药品,其中正确的是( )
| A. | 氢气中有氯化氢(氢氧化钠和氧化钙固体的混合物) | |
| B. | 二氧化碳中有少量一氧化碳(氧气) | |
| C. | 氧化钙中有杂质碳酸钙(盐酸) | |
| D. | 硫酸亚铁溶液中有硫酸铜(铁粉) |
14.“以崇尚科学为荣,以愚昧无知为耻”.下列叙述缺乏科学依据的是( )
| A. | 小孩经常咬铅笔芯,会导致铅中毒 | B. | 不可用工业酒精勾兑饮用酒 | ||
| C. | 加碘食盐的“碘”是指碘元素 | D. | 用活性炭除去冰箱的异味 |
15.推理是学习化学的一种重要方法.以下类推正确的是( )
| A. | 因为蜡烛燃烧生成CO2和H2O,则蜡烛组成里一定含有C和H | |
| B. | 酸碱中和反应有盐和水生成,则有盐和水生成的反应一定是中和反应 | |
| C. | 氧气能支持燃烧,则氧气一定具有可燃性 | |
| D. | 碱溶液呈碱性,所以呈碱性的溶液一定都是碱溶液 |