题目内容
4.如图甲所示试剂瓶中分别盛有三种常见的化学药品,图乙所示的是氧离子结构示意图.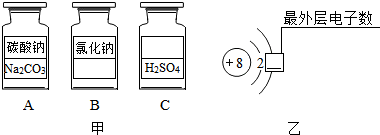
(1)图甲B瓶中的药品的化学式NaCl,C瓶中药品的名称硫酸.
(2)图乙方框内的数字是8.
(3)用化学符号和数字表示:2个金原子2Au,3个镁离子3Mg2+.
分析 (1)图甲B瓶中的药品是氯化钠,氯化钠由+1价的钠元素和-1价的氯元素组成;
图甲C瓶中的药品是H2SO4,根据化学式的读法可知其名称是硫酸.
(2)氧原子最外层有6个电子,在化学变化中易得到2个电子而形成稳定结构.
(3)表示微粒个数的数字写在符号的前面,表示离子所带电荷数的数字写在符号的右上角.
解答 解:(1)图甲B瓶中的药品是氯化钠,氯化钠由+1价的钠元素和-1价的氯元素组成,因此氯化钠的化学式为NaCl;
图甲C瓶中的药品是H2SO4,根据化学式的读法可知其名称是硫酸.
(2)氧原子最外层有6个电子,化学性质不稳定,在化学变化中易得到2个电子而形成最外层为8个电子的氧离子,因此图乙方框内的数字是8.
(3)表示微粒个数的数字写在符号的前面,表示离子所带电荷数的数字写在符号的右上角.金原子用金的元素符号来表示,因此2个金原子表示为2Au.1个镁离子带2个单位的正电荷,因此镁离子的离子符号为Mg2+,所以3个镁离子表示为3Mg2+.
故答案为:(1)NaCl;硫酸.(2)8.(3)2Au;3Mg2+.
点评 本题主要考查离子符号和化学式的书写及核外电子的排布规律,难度较小.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了下列实验(已知锌的颗粒大小相同,稀盐酸的温度均为室温).下列说法正确的是( )
| 实验① | 实验② | 实验③ |
 |  |  |
| A. | 对比实验①和②,可研究盐酸的浓度对反应剧烈程度的影响 | |
| B. | 对比实验①和②,可研究温度对反应剧烈程度的影响 | |
| C. | 对比实验②和③,可研究温度对反应剧烈程度的影响 | |
| D. | 对比实验①和③,可研究盐酸的浓度对反应剧烈程度的影响 |
9.下列四种物质中,其中有一种物质在通常条件下就能和其它三种物质发生反应,这种物质是( )
| A. | 熟石灰 | B. | 碳酸氢钠 | C. | 稀盐酸 | D. | 铁锈 |
16.下列括号中的物质是除去杂质所用药品,其中正确的是( )
| A. | 氢气中有氯化氢(氢氧化钠和氧化钙固体的混合物) | |
| B. | 二氧化碳中有少量一氧化碳(氧气) | |
| C. | 氧化钙中有杂质碳酸钙(盐酸) | |
| D. | 硫酸亚铁溶液中有硫酸铜(铁粉) |
14.“以崇尚科学为荣,以愚昧无知为耻”.下列叙述缺乏科学依据的是( )
| A. | 小孩经常咬铅笔芯,会导致铅中毒 | B. | 不可用工业酒精勾兑饮用酒 | ||
| C. | 加碘食盐的“碘”是指碘元素 | D. | 用活性炭除去冰箱的异味 |