题目内容
17.为了探究中和反应,甲、乙、丙三名同学分别进行以下实验.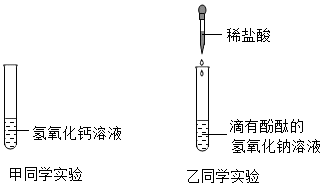
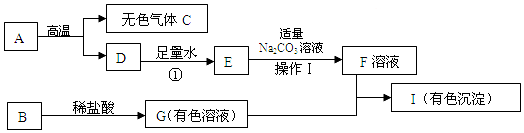
(1)甲同学向装有氢氧化钙溶液的试管中倒入一定量的稀盐酸,然后滴加酚酞试液,发现酚酞不变色,此现象能(填“能”或“不能”)说明盐酸与氢氧化钙发生了反应.
(2)乙同学向滴有酚酞的氢氧化钠溶液中逐渐加入稀盐酸,边滴加边振荡,乙同学意外发现有气泡产生,说明该氢氧化钠溶液已变质,变质的原因2NaOH+CO2=Na2CO3+H2O(用化学方程式表示).
(3)丙同学为了检验该氢氧化钠溶液的变质程度,设计实验方案并得出结论.
| 实验操作 | 实验现象 | 实验结论 |
| 取样少许于试管中,先滴加过量CaCl2溶液[或BaCl2、Ba(NO3)2、Ca(NO3)2],再滴加酚酞溶液 | 有白色沉淀生成, 酚酞溶液变红 | 氢氧化钠溶液部分变质 |
(5)丙同学要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC.
A.氢氧化钡溶液 B.硝酸钡溶液 C.氢氧化钙溶液 D.氯化钠溶液.
分析 (1)根据氢氧化钙溶液显碱性,能使无色的酚酞试液变红色进行分析;
(2)根据二氧化碳能够和氢氧化钠反应产生碳酸钠和水,写出反应的方程式;
(3)根据氢氧化钠变质生成碳酸钠,因此要检验是否变质只要检验溶液中是否含有碳酸根离子即可,检验碳酸根可用以下方法:加入盐酸产生气泡;加入氯化钙等物质产生沉淀进行检验;
(4)根据中性溶液和酸性溶液都不能使无色酚酞试液变色及反应的产物分析;
(5)根据碳酸钠能和氢氧化钡反应生成碳酸钡沉淀和氢氧化钠,碳酸钠能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠结合除杂的原则分析.
解答 解:(1)因为氢氧化钙溶液能使无色酚酞试液变红色,氢氧化钙溶液中滴加盐酸后,二者反应了反应,再滴加酚酞试液不变色,说明氢氧化钙已经参与了反应;故填:能;
(2)二氧化碳能够和氢氧化钠反应产生碳酸钠和水,故方程式为:2NaOH+CO2=Na2CO3+H2O;故填:2NaOH+CO2=Na2CO3+H2O;
(3)取少量试剂于试管中,滴加过量的过量CaCl2溶液[或BaCl2、Ba(NO3)2、Ca(NO3)2]和酚酞溶液,若出现有白色沉淀生成,酚酞溶液变红,证明氢氧化钠部分变质;故填:
| 实验操作 | 实验现象 | 实验结论 |
| 取样于试管中,先滴加过量CaCl2溶液[或BaCl2、Ba(NO3)2、Ca(NO3)2], 再滴加酚酞溶液. | 有白色沉淀生成, 酚酞溶液变红 | 氢氧化钠溶液 部分变质 |
(5)要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的氢氧化钡溶液、氢氧化钙溶液,不能选择氯化钙溶液,因为碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,因此使用氯化钙时能够带入新杂质--氯化钠,另外也不和氯化钠反应,不能起到除杂的目的.故填:AC.
点评 本题考查了学生对氢氧化钠是否变质的检验,能反映出学生对知识的掌握和实验设计能力,不仅要对氢氧化钠变质的原理要熟知,还要对反应前和反应后含有什么物质作出准确的判断,以及物质的性质,才能正确的解决.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
7.某校化学兴趣小组同学进行有关碳及其氧化物的实验(图中夹持已略去).用如图装置,在完成气密性检査后加入药品,并已在装置中充满二氧化碳.
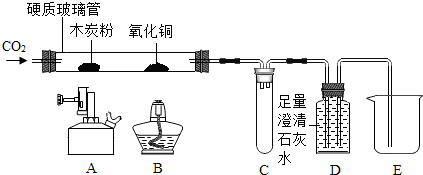
(1)填写表格中的空白内容:
(2)有同学认为该装罝需要添加尾气处理装置,你认为是否需要否(填“是”或“否”),并说明理由过量一氧化碳已收集在D中,并没有排放到空气中,不会造成污染.
(3)实验前,称得玻璃管中B处氧化铜的质量为10g,点燃B处酒精灯,加热一段时间后,玻璃管中B处剩余固体质量为8.4g.求参加反应的氧化铜的质量.(写出计算过程)

(1)填写表格中的空白内容:
| 实验步骤 | 实验现象 | 实验分析 |
| ①缓缓通入CO2,点燃A处酒精喷灯,加热一段时间 | 木炭粉减少,D中有气泡产生、澄清石灰水变浑浊且石灰水沿右侧导气管进入E | 硬质玻璃管中发生反应的化学方程式为CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,这是一个吸热(填“放热”或“吸热”)反应 |
| ②点燃B处酒精灯,加热一段时间 | B处玻璃管内黑色粉末变红 | 说明CO具有还原性 |
| ③停止通入二氧化碳,熄灭A、B两处的火焰 | C中有D中液体进入 |
(3)实验前,称得玻璃管中B处氧化铜的质量为10g,点燃B处酒精灯,加热一段时间后,玻璃管中B处剩余固体质量为8.4g.求参加反应的氧化铜的质量.(写出计算过程)
5.河水净化的主要步骤如图所示,有关说法错误的是( )
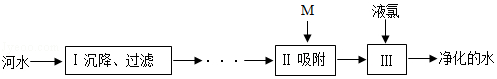

| A. | 步骤I可除去难溶性杂质 | |
| B. | 加试剂M是为了除去有颜色、气味的物质 | |
| C. | 净水的过程都属于属于物理变化 | |
| D. | 净化后的水仍是混合物 |
12.学习了二氧化锰对过氧化氢分解有催化作用的知识后,某同学想:氧化铜能否起到类似二氧化锰(MnO2)的催化剂作用呢?于是进行了以下探究.
【猜想】Ⅰ、氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ、氧化铜是反应的催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2g氧化铜,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
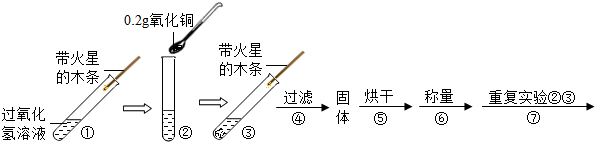
(1)填写下表:
(2)步骤①的目的是与步骤③对比.
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒;过滤不干净可能的原因是滤纸破损(写一点).
(4)过氧化氢能被氧化铜催化分解放出氧气的化学反应文字表达式为过氧化氢$\stackrel{氧化铜}{→}$水+氧气.
(5)步骤⑦实验的目的是验证化学反应前后氧化铜的化学性质不变.
(6)【拓展】除了催化剂能改变化学反应的速率,你猜想还有那些因素也可能影响化学反应的速率温度.(写一个即可)
【猜想】Ⅰ、氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ、氧化铜是反应的催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2g氧化铜,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中有气泡放出 带火星的木条复燃. | 称量CuO的质量仍为0.2g | 溶液中有气泡放出, 带火星的木条复燃 | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立. |
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒;过滤不干净可能的原因是滤纸破损(写一点).
(4)过氧化氢能被氧化铜催化分解放出氧气的化学反应文字表达式为过氧化氢$\stackrel{氧化铜}{→}$水+氧气.
(5)步骤⑦实验的目的是验证化学反应前后氧化铜的化学性质不变.
(6)【拓展】除了催化剂能改变化学反应的速率,你猜想还有那些因素也可能影响化学反应的速率温度.(写一个即可)