题目内容
9.下列框图中的物质均为初中化学常见的物质,其中A是建筑材料的主要成分,B属于氧化物,如图是它们之间的相互转化关系.请回答: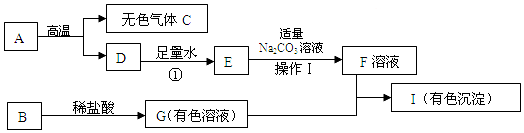
(1)得到F溶液的操作Ⅰ的名称为:过滤.
(2)若I是蓝色沉淀,请写出G+F→I的化学方程式:2NaOH+CuCl2=Cu(OH)2↓+2NaCl.
(3)若I是红褐色沉淀,请写出G+F→I的化学方程式:3NaOH+FeCl3=Fe(OH)3↓+3NaCl.
(4)指出反应①的基本类型是化合反应.
分析 根据图中的物质均为初中常见的物质,根据A是建筑材料的主要成分,所以A是碳酸钙,结合图框,碳酸钙在高温的条件下分解会生成二氧化碳和氧化钙,所以C是二氧化碳,D就是氧化钙,氧化钙和水反应会生成氢氧化钙,所以E是氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,所以F是氢氧化钠,氧化物B和盐酸反应会生成蓝色的溶液或黄色溶液,所以B是氧化铜或氧化铁,G就是氯化铜或氯化铁,氢氧化钠和氯化铜或氯化铁反应会生成有色的沉淀,所以I是蓝色沉淀氢氧化铜或红褐色沉淀氢氧化铁,然后将推出的各种物质代入转化关系中验证即可.
解答 解:图中的物质均为初中常见的物质,根据A是建筑材料的主要成分,所以A是碳酸钙,结合图框,碳酸钙在高温的条件下分解会生成二氧化碳和氧化钙,所以C是二氧化碳,D就是氧化钙,氧化钙和水反应会生成氢氧化钙,所以E是氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,所以F是氢氧化钠,氧化物B和盐酸反应会生成蓝色的溶液或黄色溶液,所以B是氧化铜或氧化铁,G就是氯化铜或氯化铁,氢氧化钠和氯化铜或氯化铁反应会生成有色的沉淀,所以I是蓝色沉淀氢氧化铜或红褐色沉淀氢氧化铁,推出的各种物质代入转化关系中经过验证均满足题意,推导合理,A是CaCO3,C是CO2;
(1)过滤的方法可以将不溶物和可溶物进行分离,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,要除去碳酸钙沉淀得到氢氧化钠溶液,可以使用过滤的方法;
(2)若I是蓝色沉淀,G就是氯化铜,则G+F→I的化学方程式:2NaOH+CuCl2=Cu(OH)2↓+2NaCl.
(3)若I是红褐色沉淀,G就是氯化铁,则G+F→I的化学方程式:3NaOH+FeCl3=Fe(OH)3↓+3NaCl.
(4)反应①为氧化钙和水反应会生成氢氧化钙,其基本类型是化合反应.
故答案为:
(1)过滤;(2)2NaOH+CuCl2=Cu(OH)2↓+2NaCl.
(3)3NaOH+FeCl3=Fe(OH)3↓+3NaCl.(4)化合反应.
点评 本题为框图式物质推断题,完成此类题目,关键是找准解题突破口,直接得出结论,然后利用物质的性质进行顺向或逆向或两边向中间推,逐一导出其他结论,最后带入验证.

 阅读快车系列答案
阅读快车系列答案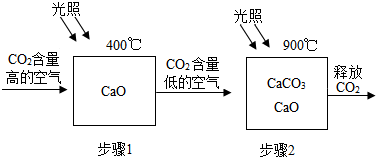
(1)步骤1的化学方程式为CaO+CO2$\frac{\underline{\;400℃\;}}{\;}$CaCO3.
(2)为确定步骤2中的碳酸钙是否完全分解,设计的实验方案如表所示:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加过量稀盐酸溶液. | 试管内有气泡产生. | 分解不完全 |
a.原料易得且可循环利用 b.充分利用太阳能 c.可全地域全天候使用
(4)CO2是宝贵的碳氧资源.CO2和H2在一定条件下可合成甲酸(HCOOH),写出此反应的化学方程式CO2+H2$\frac{\underline{\;一定条件\;}}{\;}$HCOOH.
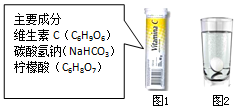 某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学对该气体的成分进行如下探究:
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学对该气体的成分进行如下探究:【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、N2.
(1)小明说:不可能含有N2,因为根据质量守恒定律可知,化学反应前后元素种类不变,反应物中不含氮元素.
(2)小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO有毒.
该小组同学认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(3)由实验①可知,该气体中肯定含有二氧化碳,写出该反应的化学方程式Ca(OH)2+CO2=CaCO3↓+H2O.
(4)由实验②不能(填“能”或“不能”)确定该气体中不含氧气,理由是若生成氧气和二氧化碳的混合物,当氧气含量过少时,带火星的木条也不能复燃.
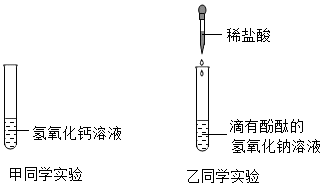
(1)甲同学向装有氢氧化钙溶液的试管中倒入一定量的稀盐酸,然后滴加酚酞试液,发现酚酞不变色,此现象能(填“能”或“不能”)说明盐酸与氢氧化钙发生了反应.
(2)乙同学向滴有酚酞的氢氧化钠溶液中逐渐加入稀盐酸,边滴加边振荡,乙同学意外发现有气泡产生,说明该氢氧化钠溶液已变质,变质的原因2NaOH+CO2=Na2CO3+H2O(用化学方程式表示).
(3)丙同学为了检验该氢氧化钠溶液的变质程度,设计实验方案并得出结论.
| 实验操作 | 实验现象 | 实验结论 |
| 取样少许于试管中,先滴加过量CaCl2溶液[或BaCl2、Ba(NO3)2、Ca(NO3)2],再滴加酚酞溶液 | 有白色沉淀生成, 酚酞溶液变红 | 氢氧化钠溶液部分变质 |
(5)丙同学要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC.
A.氢氧化钡溶液 B.硝酸钡溶液 C.氢氧化钙溶液 D.氯化钠溶液.
| A. | 变红色 | B. | 变无色 | C. | 变蓝色 | D. | 不变色 |
【提出问题】固体成分是什么?
【猜想与假设】固体成分为:A.全部是碳酸钙 B.既有碳酸钙,也有氧化钙 C.全部是氧化钙
【查阅资料】
①氧化钙与水反应生成氢氧化钙;
②氢氧化钙的水溶液能使无色酚酞试液变红;
③氧化钙与稀盐酸反应会生成氯化钙溶液.
【设计并完成实验】
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体于试管中,加适量水振荡后静置,在滴几滴无色酚酞试液 | 溶液变红 | 说明固体成分中一定含有氧化钙 |
| (2)再取少量固体于另一试管中滴加过量稀盐酸 | 有气泡生成 | 说明固体成分中一定含有碳酸钙 |
| A. | 氢气燃烧放出大量热 | B. | 氢气是密度最小的气体 | ||
| C. | 氢气具有可燃性 | D. | 氢气燃烧产生淡蓝色火焰 |

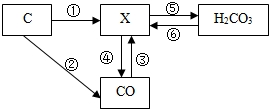 碳和部分碳的化合物间转化关系如图所示.
碳和部分碳的化合物间转化关系如图所示.