题目内容
7.通过化学学习,你应该知道有多种途径可以制取氧气.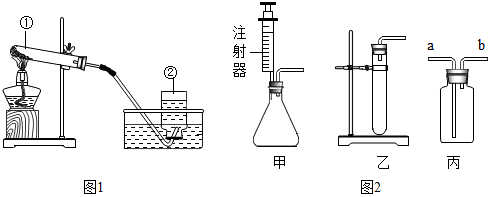
(1)用化学方程式式表示下列制取氧气的方法;
A、分离液态空气B、2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2 ↑C、2KMnO$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ D、2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑E.2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2 ↑
(2)写出如图1所示装置中标号仪器的名称:①试管②集气瓶;
(3)实验结束,停止加热时要先把导管移出水面,其理由是防止水倒流入试管,引起试管的炸裂.
(4)若用分解过氧化氢来制取氧气,可供选用的装置如图2所示:要在实验时可以方便的添加液体反应物并得到平稳的氧气流,应选用的发生装置是甲(选填“甲”或“乙”);若用丙装置收集生成的氧气,气体应从a(“a”或“b”)端导入.
分析 (1)根据制取氧气的方法及反应原理写出化学方程式即可;
(2)根据常见仪器的名称进行分析;
(3)实验室制取氧气的步骤及实验中应注意的事项进行分析解答;
(4)根据注射器、分液漏斗能够控制液体药品的流量选择发生装置即可;根据氧气的密度比空气大进行分析.
解答 解:(1)过初中化学的学习,我们知道,通过多种途径可制取氧气,如:A、分离液态空气、B、加热分解KClO3、D.加热分解KMnO4、C、分解H2O2、E、电解水;氯酸钾在二氧化锰和加热的条件下生成氯化钾和氧气,化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2 ↑;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,化学方程式为:2KMnO$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;水在通电的条件下生成氢气和氧气,化学方程式为:2H2O $\frac{\underline{\;通电\;}}{\;}$2H2↑+O2 ↑;
故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2 ↑;2KMnO$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;2H2O $\frac{\underline{\;通电\;}}{\;}$2H2↑+O2 ↑;
(2)图1所示装置中标号仪器的名称:①是试管,②是集气瓶;
故答案为:试管;集气瓶;
(3)实验结束后为防止水倒流入试管,引起试管的炸裂,必须先将导管移出水面,后熄灭酒精灯;
故答案为:防止水倒流入试管,引起试管的炸裂;
(4)根据题干信息(方便添加液体)可知甲符合条件,因为甲有一个注射器注射液体,可以随时添加液体;若用丙装置收集生成的氧气,由于氧气的密度比空气大,气体应从a端导入.
故答案为:甲;a.
点评 本考点主要考查氧气的制取方法、实验中的注意事项,同时也考查了化学方程式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

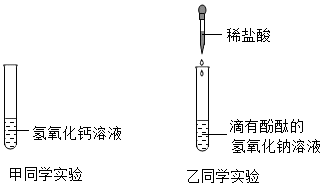
(1)甲同学向装有氢氧化钙溶液的试管中倒入一定量的稀盐酸,然后滴加酚酞试液,发现酚酞不变色,此现象能(填“能”或“不能”)说明盐酸与氢氧化钙发生了反应.
(2)乙同学向滴有酚酞的氢氧化钠溶液中逐渐加入稀盐酸,边滴加边振荡,乙同学意外发现有气泡产生,说明该氢氧化钠溶液已变质,变质的原因2NaOH+CO2=Na2CO3+H2O(用化学方程式表示).
(3)丙同学为了检验该氢氧化钠溶液的变质程度,设计实验方案并得出结论.
| 实验操作 | 实验现象 | 实验结论 |
| 取样少许于试管中,先滴加过量CaCl2溶液[或BaCl2、Ba(NO3)2、Ca(NO3)2],再滴加酚酞溶液 | 有白色沉淀生成, 酚酞溶液变红 | 氢氧化钠溶液部分变质 |
(5)丙同学要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC.
A.氢氧化钡溶液 B.硝酸钡溶液 C.氢氧化钙溶液 D.氯化钠溶液.
| A. | (a-b-c) g | B. | (a-b) g | C. | (a+b-c) g | D. | (a-b+c) g |
| A. | 氢气燃烧放出大量热 | B. | 氢气是密度最小的气体 | ||
| C. | 氢气具有可燃性 | D. | 氢气燃烧产生淡蓝色火焰 |
| A. | 用100ml的量筒量取6.33ml的水 | |
| B. | 学生分组实验时,用燃着的酒精灯去引燃另一只酒精灯 | |
| C. | 为了节约药品,用剩的药品应当放回原试剂瓶 | |
| D. | 把红热的木炭插入盛有氧气的集气瓶中时,要由瓶口向下缓慢插入 |
| A. | 本饮料不含任何化学物质,绝对健康安全 | |
| B. | 提倡生态农业,禁止使用农药、化肥 | |
| C. | 限制使用塑料袋,减少白色污染 | |
| D. | 为促进农作物增产,不需控制二氧化碳的排放 |
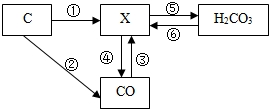 碳和部分碳的化合物间转化关系如图所示.
碳和部分碳的化合物间转化关系如图所示.