题目内容
12.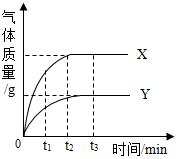 等质量的X、Y两种金属分别和足量的同体积、同浓度的盐酸反应,产生气体的质量与时间的关系如图所示.下列说法中不正确的是( )
等质量的X、Y两种金属分别和足量的同体积、同浓度的盐酸反应,产生气体的质量与时间的关系如图所示.下列说法中不正确的是( )| A. | t1时,产生气体的质量:X>Y | B. | t2时,消耗金属的质量:X>Y | ||
| C. | 从图中可以看出金属Y比X活泼 | D. | t3时,消耗盐酸的质量:X=Y |
分析 A、根据图中提供的数据可以判断产生气体质量的多少;
B、虽然产生的气体质量不相等,消耗的金属质量可能相等;
C、根据相同的时间内产生的氢气多少分析;
D、产生氢气质量相等时,消耗盐酸质量相等,产生氢气质量不相等时,消耗的盐酸质量不相等.
解答 解:A、t1时,产生气体的质量是X>Y,故A正确;
B、由图可知,t2 时,X已经消耗完,Y还没有消耗完,又开始时两者的质量相等且酸是过量的,所以t2时消耗金属的质量:X>Y,故正确.
C、由图可知,相同的时间内X产生的氢气比Y多,说明金属的活泼性X>Y,故C不正确;
D、由题干可知,金属的质量相等,且酸是足量的,所以最后金属全部反应完,图示中t3 时刻两者的气体质量不再变化,说明金属已经完全反应,又金属的质量相等,所以消耗金属的质量X=Y,故正确;
故选:C.
点评 由图中数据可知,X金属与盐酸反应需要的时间短,说明X比Y活泼,至于X与Y的质量关系,可以根据是否完全反应进行判断.

练习册系列答案
 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
20.我们能闻到臭豆腐的特殊香味是因为( )
| A. | 分子之间有间隔 | B. | 分子在不断运动 | C. | 分子的质量很小 | D. | 分子的体积很小 |
4.下列说法正确的是( )
| A. | 物质和氧气发生的反应是氧化反应,所以发生氧化反应一定有氧气参加 | |
| B. | 合金的硬度大于各成分金属,所以黄铜的硬度大于紫铜 | |
| C. | 可燃物燃烧时温度需要达到着火点,所以可燃物的温度达到着火点一定能燃烧 | |
| D. | 单质一定是由一种元素组成的,所以由一种元素组成的物质一定是单质 |
2.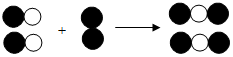 如图,该图能体现的知识有( )
如图,该图能体现的知识有( )
①质量守恒定律;
②化合物分子是由不同原子构成的;
③在化学反应中分子的种类发生了改变;
④该反应可能是氢气与氧气的反应.
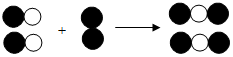 如图,该图能体现的知识有( )
如图,该图能体现的知识有( )①质量守恒定律;
②化合物分子是由不同原子构成的;
③在化学反应中分子的种类发生了改变;
④该反应可能是氢气与氧气的反应.
| A. | ①②③④ | B. | ①②③ | C. | ②③④ | D. | ②③ |
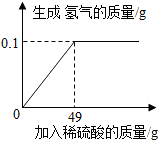 小王同学想测定某Cu-Zn合金中锌的质量,取合金粉末10g,向其中逐渐加入一定溶质质量分数的稀硫酸,所加稀硫酸与生成氢气的质量关系如图所示.请完成下列分析及计算:
小王同学想测定某Cu-Zn合金中锌的质量,取合金粉末10g,向其中逐渐加入一定溶质质量分数的稀硫酸,所加稀硫酸与生成氢气的质量关系如图所示.请完成下列分析及计算: