题目内容
11.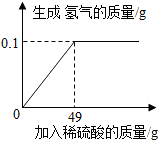 小王同学想测定某Cu-Zn合金中锌的质量,取合金粉末10g,向其中逐渐加入一定溶质质量分数的稀硫酸,所加稀硫酸与生成氢气的质量关系如图所示.请完成下列分析及计算:
小王同学想测定某Cu-Zn合金中锌的质量,取合金粉末10g,向其中逐渐加入一定溶质质量分数的稀硫酸,所加稀硫酸与生成氢气的质量关系如图所示.请完成下列分析及计算:(1)反应生成的氢气总质量为0.1g.
(2)计算合金中锌的质量.
分析 (1)根据图中的信息可知氢气的质量.
(2)利用锌与硫酸反应的化学方程式,根据氢气的质量求出锌的质量.
解答 解:(1)由图可知,完全反应后生成氢气的质量为0.1g.
(2)设该合金中锌的质量为 x
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.1g
$\frac{65}{x}$=$\frac{2}{0.1g}$
x=3.25g
故答案为:(1)0.1;
(2)3.25g.
点评 本题考查根据化学方程式的简单计算,已知生成物的质量求反应物的质量,解题的关键是正确的对图象意义的分析.

练习册系列答案
 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案
相关题目
1.下列实验操作中,正确的是( )
| A. | 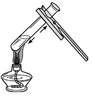 加热液体 | B. | 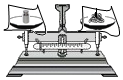 称量固体 | C. | 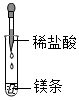 滴加液体 | D. |  过滤 |
19.下列方程式书写正确的是( )
| A. | 2Fe+6HCl═FeCl3+3H2↑ | B. | 2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2↑+O2↑ | ||
| C. | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | D. | Cu+AgNO3═CuNO3+Ag |
16.下列物质均为有机物的是( )
| A. | 淀粉、甲烷 | B. | 氨气、酒精 | C. | 食醋、金刚石 | D. | 碳酸钠、葡萄糖 |
3.自然界中的物质是千变万化的,下列现象中属于物理变化的是( )
| A. | 露水消失 | B. | 火山爆发 | C. | 食物变质 | D. | 铁制品生锈 |
12.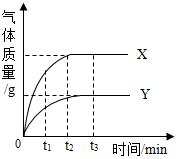 等质量的X、Y两种金属分别和足量的同体积、同浓度的盐酸反应,产生气体的质量与时间的关系如图所示.下列说法中不正确的是( )
等质量的X、Y两种金属分别和足量的同体积、同浓度的盐酸反应,产生气体的质量与时间的关系如图所示.下列说法中不正确的是( )
 等质量的X、Y两种金属分别和足量的同体积、同浓度的盐酸反应,产生气体的质量与时间的关系如图所示.下列说法中不正确的是( )
等质量的X、Y两种金属分别和足量的同体积、同浓度的盐酸反应,产生气体的质量与时间的关系如图所示.下列说法中不正确的是( )| A. | t1时,产生气体的质量:X>Y | B. | t2时,消耗金属的质量:X>Y | ||
| C. | 从图中可以看出金属Y比X活泼 | D. | t3时,消耗盐酸的质量:X=Y |