题目内容
5.现代生活节奏压力大,一些包装精美及口味独特的小食品既方便了我们的生活又调适了我们的心情.选购包装(或灌装)食品时,在配料中我们常常会看到”山梨酸“或”山梨酸钾“的字样,人们往往会误认为可能是梨的成分,其实它们是一些常见的食品防腐剂.资料显示:
a.山梨酸的化学式为C5H7COOH,无色粉末,无毒,在20℃时溶解度为0.18g,100℃时为3.8g,易露于空气中易被氧化而变色,有很强的抑制腐败菌和霉菌作用,可被人体的代谢系统吸收而转化为二氧化碳和水.
b.山梨酸钾的化学式为C5H7COOK
试根据其组成与结构,回答下列问题:
(1)山梨酸钾的组成共有三种非金属元素,该物质属于有机物(请从“混合物”、“单质”“氧化物”“有机物”“酸”中选填一项).
(2)山梨酸中碳元素和氢元素的质量比为9:1(填最简整数比).
(3)关注食品安全,关爱身体健康已经成为社会共识.下列观点中,错误的是A
A.食品添加剂都会对人体造成伤害
B.食用腐烂变质水果蔬菜有害健康
C.可以适量服用保健品补充身体缺少的营养元素.
分析 (1)根据山梨酸钾化学式进行分析其元素组成即可;根据有机物的概念来分析;
(2)据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行分析解答;
(3)A.根据食品添加剂应合理使用进行分析;
B、根据腐烂变质水果蔬菜中有毒物质进行分析;
C、根据保健品与人体健康的关系进行分析.
解答 解:(1)根据化学式可知山梨酸钾是由碳、氢、钾、氧四种元素组成,山梨酸钾的组成共有三种非金属元素,该物质属于;山梨酸钾是含碳元素的化合物,属于有机物;
(2)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得C6H8O2中C、H元素的质量比为(12×6):8=9:1;
(3)A.食品添加剂是为改善食品色、香、味等品质,应合理使用食品添加剂,且有些食品添加剂对人体无害,如蔗糖、果糖等是天然的食品添加剂,对人体无害;故A错误;
B、腐烂变质的水果蔬菜产生了有害物质,不能食用,故B正确;
C、可以适量服用保健品补充身体缺少的营养元素,故C正确.
故答案为:(1)三;有机物;(2)9:1;(3)A.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化学知识也是重要的中考热点之一.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案
相关题目
15.在日常生活和工农业生产中,溶液有着广泛的应用.比如,氨碱工业用到的是饱和食盐水,医疗上使用的则是0.9%的生理盐水.请按要求设计并完成以下实验:
实验用品:氯化钠溶液、氯化钠、硝酸钾、蒸馏水、烧杯、试管、玻璃棒、药匙.
探究实验一:澄清透明的氯化钠溶液是否是饱和溶液
探究实验二:将不饱和氯化钠溶液变为饱和溶液并探究饱和氯化钠溶液还能否溶解硝酸钾
实验用品:氯化钠溶液、氯化钠、硝酸钾、蒸馏水、烧杯、试管、玻璃棒、药匙.
探究实验一:澄清透明的氯化钠溶液是否是饱和溶液
| 实验步骤 | 实验现象 | 实验结论 |
| 取一只试管倒入约5mL氯化钠溶液,用药匙加入少量氯化钠固体,振荡,观察现象. | 氯化钠固体溶解 | 是不饱和氯化钠溶液 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取一只试管倒入约10mL不饱和氯化钠溶液,用药匙加入适量氯化钠固体,振荡 | 氯化钠不能再溶解 | NaCl不饱和溶液变为饱和溶液 |
| 取一只试管倒入约10mL饱和氯化钠溶液,用药匙加入适量硝酸钾固体,振荡 | 硝酸钾溶解 | 饱和氯化钠溶液能够溶解硝酸钾 |
20.要除去下列物质中的少量杂质(括号内为杂质),下列实验方案设计中合理的是( )
| A. | BaSO4(BaCO3):加水,过滤 | |
| B. | Cu(CuO):过量稀盐酸,过滤 | |
| C. | NaCl溶液(Na2CO3):适量硝酸钙溶液,过滤 | |
| D. | CO(CO2):Fe2O3,高温 |
10.人类利用金属矿物历史久远.
(1)现代冶炼技术用CO与赤铁矿石反应来冶炼生铁,请写出该反应的化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)某矿石由MgO、Fe2O3、CuO和SiO2组成,用它制备氢氧化镁的流程示意图如图所示:
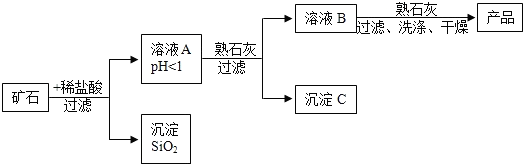
①溶液A中共含有四种阳离子;
②在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子转化为沉淀.该实验条件下,使金属阳离子沉淀的相关pH数据见下表.为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可容许的范围为6.7~8.6;
③溶液B中一定含有的溶质为MgCl2、CaCl2(填化学式).
(1)现代冶炼技术用CO与赤铁矿石反应来冶炼生铁,请写出该反应的化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)某矿石由MgO、Fe2O3、CuO和SiO2组成,用它制备氢氧化镁的流程示意图如图所示:

①溶液A中共含有四种阳离子;
②在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子转化为沉淀.该实验条件下,使金属阳离子沉淀的相关pH数据见下表.为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可容许的范围为6.7~8.6;
| 氢氧化物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 4.2 | 8.6 |
| 完全沉淀的pH | 3.2 | 6.7 | 11.1 |
 金属是重要的资源,在日常生活中已得到越来越广泛的应用.
金属是重要的资源,在日常生活中已得到越来越广泛的应用.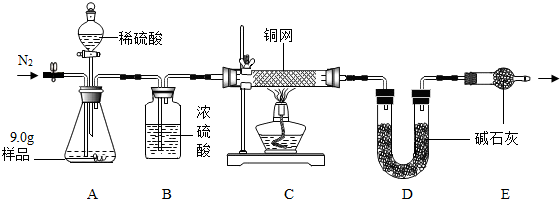
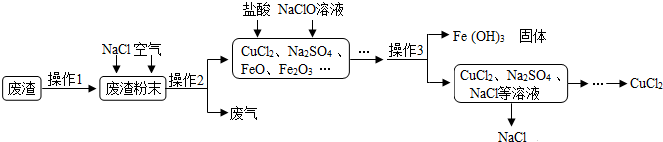
 科学严谨的态度,安全规范的操作是成功进行化学实验的保障.
科学严谨的态度,安全规范的操作是成功进行化学实验的保障.