题目内容
16. 金属是重要的资源,在日常生活中已得到越来越广泛的应用.
金属是重要的资源,在日常生活中已得到越来越广泛的应用.(1)铜常用于制作导线,因为其具有良好的导电性.
(2)将纯铝和铝合金相互刻画,纯铝上留下明显划痕,说明铝合金的硬度大于纯铝的硬度.
(3)对汽车部分钢铁部件进行喷漆可以防止其生锈,原因是隔绝氧气和水.
(4)如图,向一定量AgNO3溶液中加入铜和锌的混合粉末,充分反应后过滤,得溶液甲和固体乙.
①若乙中含有锌、铜、银三种固体,则溶液甲中所含的金属离子符号为Zn2+此时向固体乙中加入稀盐酸,发生反应的化学方程式为Zn+2HCl═ZnCl2+H2↑,该反应类型为置换反应.
②若溶液甲显蓝色,是因为Cu+2AgNO3═2Ag+Cu(NO3)2(用化学反应方程式表示),此时固体乙中一定含有的物质是银.
分析 (1)根据同的性质和用途分析;
(2)根据纯铝和铝合金的硬度分析;
(3)根据防止生锈的原理分析回答;
(4)根据在金属活动性顺序中,排在前面的金属可以把位于它后面的金属从其盐溶液中置换出来,可简记为“前置后,盐可溶”进行分析.
解答 解:(1)铜常用于制作导线,因为其具有良好的导电性.
(2)将纯铝和铝合金相互刻画,纯铝上留下明显划痕,说明铝合金的硬度大于纯铝的硬度.
(3)对汽车部分钢铁部件进行喷漆可以防止其生锈,原因是隔绝氧气和水;
(4)在金属活动顺序表中,金属的活动性顺序是锌>铜>银.向一定量AgNO3溶液中加入铜和锌的混合粉末时,锌先与硝酸银反应,当锌反应完后,铜再与硝酸银反应.
①若乙中含有锌、铜、银三种固体,说明了溶液中没有硝酸银、硝酸铜,则溶液甲中所含的金属离子符号为:Zn2+,此时向固体乙中加入稀盐酸,锌能与发生反应,化学方程式为:Zn+2HCl═ZnCl2+H2↑,该反应是一种单质与一种化合物反应生成了另一种单质和另一种化合物,属于置换反应;
②若溶液甲显蓝色,说明了铜与于硝酸银反应生成了硝酸铜,化学方程式为:Cu+2AgNO3═2Ag+Cu(NO3)2,此时固体乙中一定含有的物质是银.
故答案为:(1)掉电性;(2)铝合金的硬度大于纯铝的硬度;(3)隔绝氧气和水;(4)①Zn2+,Zn+2HCl═ZnCl2+H2↑,置换;②Cu+2AgNO3═2Ag+Cu(NO3)2,银.
点评 本题考查了金属活动性顺序的应用,难度不大,完成此题,可以依据金属活的知识分析回答.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
6.下列有关空气及其成分的说法有
①空气是一种混合物
②空气中氮气与氧气的质量比约为4:1
③一氧化碳、二氧化硫、二氧化氮是形成酸雨的污染物
④空气中的二氧化碳主要来自植物的光合作用
⑤氮气可用作焊接金属时的保护气
⑥稀有气体在通电时能发出不同颜色的光,可制成电光源.
其中正确的是( )
①空气是一种混合物
②空气中氮气与氧气的质量比约为4:1
③一氧化碳、二氧化硫、二氧化氮是形成酸雨的污染物
④空气中的二氧化碳主要来自植物的光合作用
⑤氮气可用作焊接金属时的保护气
⑥稀有气体在通电时能发出不同颜色的光,可制成电光源.
其中正确的是( )
| A. | ①⑤⑥ | B. | ①②④⑤⑥ | C. | ①③④⑤ | D. | ②④⑤⑥ |
7.下列图示的实验操作正确的是( )
| A. | 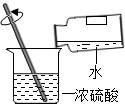 稀释浓硫酸 | B. |  测定溶液pH | ||
| C. |  过滤 | D. | .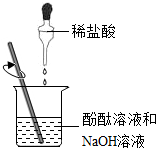 验证中和反应 |
11.某白色固体A可能含有碳酸钠、氯化钡(水溶液呈中性)、氢氧化钠中的一种或几种,进行如下实验:
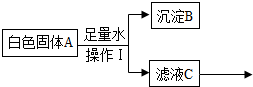
完成下列填空:
①根据上述实验分析,A中一定含有的物质是碳酸钠、氯化钡,写出生成B的化学方程式:Na2CO3+BaCl2═BaCO3↓+2NaCl.
②为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成如表.

完成下列填空:
①根据上述实验分析,A中一定含有的物质是碳酸钠、氯化钡,写出生成B的化学方程式:Na2CO3+BaCl2═BaCO3↓+2NaCl.
②为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成如表.
| 实验操作 | 现象 | 结论 |
| 向滤液C中加入足量的氯化钡溶液,充分反应后,静置,取上层清液滴加无色酚酞 | 无色酚酞变红色 | A中有氢氧化钠 |
1.KNO3与NH4Cl两种物质的溶解度曲线如图所示,下列说法错误的是( )


| A. | t1℃时用等质量的固体配制饱和溶液,NH4Cl溶液质量更大 | |
| B. | t2℃时两种饱和溶液中溶质的质量分数一定相等 | |
| C. | t3℃时KNO3的溶解度大于NH4Cl的溶解度 | |
| D. | 两种饱和溶液从t2℃降到t1℃时,均有晶体析出 |
8.下列各组离子可在同一溶液中大量共存的是( )
| A. | H+ SO42- K+ CO32- | B. | Mg2+ Cl- OH- Na+ | ||
| C. | Fe3+ SO42- H+ Cl- | D. | Na+ Ba2+ NO3- SO42- |
14.对于Cl和Cl-的说法,不正确的是( )
| A. | 属于同一种元素 | B. | 质子数相同 | ||
| C. | 核外电子数相同 | D. | 具有相同的电子层数 |
