题目内容
12.某同学利用括号内的操作或物质进行实验,设计的下列各实验方案中,可行的是( )| A. | 分离氧化钙中混有的碳酸钙粉末(加水溶解,过滤,蒸发) | |
| B. | 鉴别固体:氢氧化钠.氯化钠.硝酸铵(水) | |
| C. | 除去二氧化碳中混有少量的一氧化碳 (点燃) | |
| D. | 验证铁.铜.银的金属活动性顺序(硫酸铜溶液.银丝.硝酸亚铁溶液) |
分析 氧化钙和水反应生成氢氧化钙;
氢氧化钠溶于水放热,氯化钠溶于水无明显现象,硝酸铵溶于水吸收热量;
二氧化碳不能燃烧,不支持燃烧;
铁比铜活泼,铜比银活泼.
解答 解:A、氧化钙和水反应生成氢氧化钙,因此不能用加水溶解,过滤,蒸发的方法分离氧化钙中混有的碳酸钙粉末;
B、氢氧化钠溶于水放热,氯化钠溶于水无明显现象,硝酸铵溶于水吸收热量,因此可以用溶于水的方法鉴别固体氢氧化钠、氯化钠和硝酸铵;
C、二氧化碳不能燃烧,不支持燃烧,因此不能用点燃的方法除去二氧化碳中混有少量的一氧化碳;
D、把银丝伸入硫酸铜溶液和硫酸亚铁溶液中时,都无明显现象,因此不能用硫酸铜溶液.银丝.硝酸亚铁溶液验证铁、铜、银的活动性顺序.
故选:B.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
3.根据质量守恒定律判断,镁条在氧气中完全燃烧,生成物的总质量( )
| A. | 一定大于镁条的质量 | B. | 一定小于镁条的质量 | ||
| C. | 一定等于镁条的质量 | D. | 不能确定 |
4.由NaHS、MgSO4、NaHSO3组成的混合物中,已知S元素的质量分数w(S)=a%,则O元素的质量分数w(O)为( )
| A. | 1.25a% | B. | 1.75a% | C. | 1-1.75a% | D. | 无法计算 |
1.“塑化剂”是一种重要的化工原料,属2B类致癌物,曾被添加到食品中,造成了“塑化剂”风暴.已知“塑化剂”的化学式为C24H38O4.下列说法错误的是( )
| A. | 该“塑化剂”中碳、氢、氧三种元素的质量比为12:19:2 | |
| B. | 该“塑化剂”中碳的质量分数为73.8% | |
| C. | 该“塑化剂”属有机物 | |
| D. | 食品添加剂要严格按照国家规定标准进行使用 |
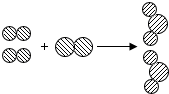 如图所示,
如图所示, 表示氢原子,
表示氢原子, 表示氧原子.试从物质组成、分子构成、物质变化的角度各说明一种观点.
表示氧原子.试从物质组成、分子构成、物质变化的角度各说明一种观点. 如图一软塑料瓶中充满二氧化碳气体,向瓶中倒入少量水后迅速拧紧瓶盖,振荡,观察到瓶子瘪了,再倒入紫色石蕊试液,观察到溶液变为红色.如果倒入相同体积的澄清石灰水,发现瓶子更瘪.用化学方程式觯释出现上述现象的原因.CO2+H2O=H2CO3,Ca(OH)2+CO2=CaCO3↓+H2O.
如图一软塑料瓶中充满二氧化碳气体,向瓶中倒入少量水后迅速拧紧瓶盖,振荡,观察到瓶子瘪了,再倒入紫色石蕊试液,观察到溶液变为红色.如果倒入相同体积的澄清石灰水,发现瓶子更瘪.用化学方程式觯释出现上述现象的原因.CO2+H2O=H2CO3,Ca(OH)2+CO2=CaCO3↓+H2O.