题目内容
实验室中有两瓶失去标签的无色溶液,只知道它们是氯化钠溶液和稀硫酸.应用你所学化学知识,试写出三种能分别将两溶液鉴别开的化学试剂(要求三种方法实验现象不同):① ;② ;③ .
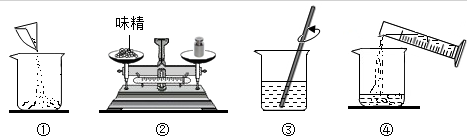
如果小王仅使用了酒精灯和玻璃棒两种仪器,就把这两种无色溶液区分开来了.请你猜测一下他的做法(简要叙述操作方法及判断方法): .
如果小王仅使用了酒精灯和玻璃棒两种仪器,就把这两种无色溶液区分开来了.请你猜测一下他的做法(简要叙述操作方法及判断方法):
考点:酸、碱、盐的鉴别
专题:物质的鉴别题
分析:首先分析两种物质的组成和类别,氯化钠是盐,硫酸是酸;鉴别硫酸可根据其酸性及硫酸根的性质进行试剂的选;题意要求三种方法的现象不一,常见的现象主要颜色、生成沉淀或放出气体.物理方法主要是使用了酒精灯和玻璃棒两种仪器,根据物质的挥发性解答.
解答:解:①因为硫酸呈酸性,所有可用紫色石蕊试液检验,变红色,而氯化钠不变色.
②因为硫酸是酸可和活泼的金属反应放出氢气,可用锌粒进行检验,和硫酸反应有气泡产生.
③因为硫酸钡是沉淀,所有可用BaCl2溶液进行检验,和硫酸反应有白色沉淀产生,氯化钠没有.
同理还可选用碳酸钠、氧化铜、氢氧化铜等试剂都可鉴别出.
因盐酸易挥发,蒸发后不留任何痕迹;氯化钠蒸发水分后会留下白色固体;
故答案为:①石蕊试液; ②锌粒;③氯化钡溶液;用玻璃棒分别蘸取两种样品放在酒精灯火焰上灼烧,玻璃棒上有白色固体出现的原样品是氯化钠溶液,没有白色固体出现的原样品是稀盐酸.
②因为硫酸是酸可和活泼的金属反应放出氢气,可用锌粒进行检验,和硫酸反应有气泡产生.
③因为硫酸钡是沉淀,所有可用BaCl2溶液进行检验,和硫酸反应有白色沉淀产生,氯化钠没有.
同理还可选用碳酸钠、氧化铜、氢氧化铜等试剂都可鉴别出.
因盐酸易挥发,蒸发后不留任何痕迹;氯化钠蒸发水分后会留下白色固体;
故答案为:①石蕊试液; ②锌粒;③氯化钡溶液;用玻璃棒分别蘸取两种样品放在酒精灯火焰上灼烧,玻璃棒上有白色固体出现的原样品是氯化钠溶液,没有白色固体出现的原样品是稀盐酸.
点评:本题主要考查学生根据物质性质进行鉴别的内容,对于本题还要注意审题,题干要求所举三个试剂反应后的现象不同,这是本题的难点.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
把足量的铁粉分别加入到含有下列各组物质的溶液中充分反应后过滤,滤液中只有一种溶质的是( )
| A、ZnSO4、CuSO4 |
| B、HCl、CuCl2 |
| C、Al(NO3)3、Hg(NO3)2 |
| D、Cu(NO3)2、MgSO4 |
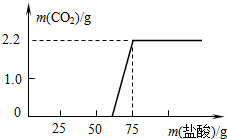 探究实验室中久置的NaOH的变质程度
探究实验室中久置的NaOH的变质程度