题目内容
味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是C5H8NO4Na,易溶于水,与AgNO3不反应),另外还含有NaCl(其他成分不考虑).请回答下列问题: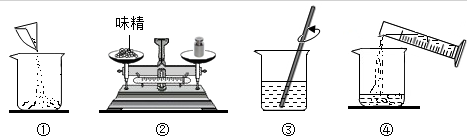
(1)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是 .(填字母)
A.10mL B.50mL C.100mL
(2)如图是配制过程,正确的操作顺序为 .(填序号)
(3)为测定味精中NaCl的质量分数,进行如下实验:
①向所配制的50g溶液中加入过量的 溶液(填化学式)充分反应.
②然后进行 (填操作名称)、洗涤、干燥后称量AgCl固体.
③在其他操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液的谷氨酸钠质量分数 (填“偏大”、“偏小”或“无影响”),则测得的样品中氯化钠的质量分数 (填“偏大”、“偏小”或“无影响”).
④经精确测定AgCl沉淀的质量为2.87g,则该味精中NaCl的质量分数为 .(计算结果保留一位小数)

(1)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是
A.10mL B.50mL C.100mL
(2)如图是配制过程,正确的操作顺序为
(3)为测定味精中NaCl的质量分数,进行如下实验:
①向所配制的50g溶液中加入过量的
②然后进行
③在其他操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液的谷氨酸钠质量分数
④经精确测定AgCl沉淀的质量为2.87g,则该味精中NaCl的质量分数为
考点:实验探究物质的组成成分以及含量,一定溶质质量分数的溶液的配制,盐的化学性质,根据化学反应方程式的计算
专题:科学探究
分析:(1)根据溶液质量=溶质质量+溶剂质量,由5.0g味精配制成50g溶液,求出配制时所需水的量,然后选择量取蒸馏水的量筒;
(2)根据使用固体物质配制溶液的步骤:计算、称量、溶解,判断实验操作图中操作的顺序;
(3)①根据溶液中的氯化钠与硝酸银溶液能发生化学反应,生成氯化银白色沉淀和硝酸钠进行解答;
②根据过滤可用于分离难溶性与可溶性固体进行解答;
③根据仰视刻度量取蒸馏水可以造成蒸馏水的体积增大进行解答;
④根据氯化银的质量求出氯化钠的质量,然后求出味精中NaCl的质量分数即可.
(2)根据使用固体物质配制溶液的步骤:计算、称量、溶解,判断实验操作图中操作的顺序;
(3)①根据溶液中的氯化钠与硝酸银溶液能发生化学反应,生成氯化银白色沉淀和硝酸钠进行解答;
②根据过滤可用于分离难溶性与可溶性固体进行解答;
③根据仰视刻度量取蒸馏水可以造成蒸馏水的体积增大进行解答;
④根据氯化银的质量求出氯化钠的质量,然后求出味精中NaCl的质量分数即可.
解答:解:(1)取5.0g味精配制成50g溶液,则需要水的质量50g-5.0g=45g,45g水的体积为45mL,因此需要选择50mL的量筒.故选B;
(2)图①为称量完毕的味精倒入烧杯,图②为称量味精的质量,图③为进行溶解,图④为量取水后倒入盛有味精的烧杯,因此,正确的操作顺序为②①④③,故答案为:②①④③;
(3)①溶液中的氯化钠与硝酸银溶液能发生化学反应,生成氯化银白色沉淀和硝酸钠,所以向所配制的50g溶液中加入过量的硝酸银溶液充分反应;故填:AgNO3;
②过滤可用于分离难溶性与可溶性固体,所以进行过滤、洗涤、干燥后称量AgCl固体;故填:过滤;
③仰视刻度量取蒸馏水可以造成蒸馏水的体积增大,所以仰视刻度量取蒸馏水,则所配制溶液的谷氨酸钠质量分数偏小,但是对样品中氯化钠的质量分数不影响;故填:偏小;无影响;
④设味精中NaCl的质量为x.
AgNO3+NaCl═AgCl↓+NaNO3
58.5 143.5
x 2.87g
=
x=1.17g
该味精中NaCl的质量分数=
×100%=23.4%
答:该味精中NaCl的质量分数为23.4%.
故填:23.4%.
(2)图①为称量完毕的味精倒入烧杯,图②为称量味精的质量,图③为进行溶解,图④为量取水后倒入盛有味精的烧杯,因此,正确的操作顺序为②①④③,故答案为:②①④③;
(3)①溶液中的氯化钠与硝酸银溶液能发生化学反应,生成氯化银白色沉淀和硝酸钠,所以向所配制的50g溶液中加入过量的硝酸银溶液充分反应;故填:AgNO3;
②过滤可用于分离难溶性与可溶性固体,所以进行过滤、洗涤、干燥后称量AgCl固体;故填:过滤;
③仰视刻度量取蒸馏水可以造成蒸馏水的体积增大,所以仰视刻度量取蒸馏水,则所配制溶液的谷氨酸钠质量分数偏小,但是对样品中氯化钠的质量分数不影响;故填:偏小;无影响;
④设味精中NaCl的质量为x.
AgNO3+NaCl═AgCl↓+NaNO3
58.5 143.5
x 2.87g
| 58.5 |
| x |
| 143.5 |
| 2.87g |
x=1.17g
该味精中NaCl的质量分数=
| 1.17g |
| 5.0g |
答:该味精中NaCl的质量分数为23.4%.
故填:23.4%.
点评:掌握溶解、过滤、蒸发等实验的操作技能;理解过滤法分离混合物的原理;体会过滤的原理在生活生产等社会实际中的应用.本题具有较大的综合性,在解答时需要涉及较多的基础知识,因此,需要足够的耐心和毅力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法不正确的是( )
| A、饼干在空气中放置一段时间后变软,说明空气中含有水蒸气 |
| B、常用氮气做食品保护气,是由于氮气的化学性质不活泼 |
| C、空气中氧气的质量分数占21%,工业上可用分离液态空气的方法制取氧气 |
| D、稀有气体又叫惰性气体,常用作保护气 |
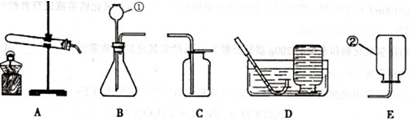

 若分解过氧化氢制取氧气,供选用的装置如下:
若分解过氧化氢制取氧气,供选用的装置如下: