题目内容
登山队员常用的能源是氢化钙(CaH2)固体,用它和水反应生成氢氧化钙[Ca(OH)2]和氢气,氢气供燃烧之需.请回答下列问题.
(1)写出氢化钙与水反应的化学方程式
(2)现有875g氢化钙固体(含CaH296%),与足量水反应可生成多少克氢气?
(1)写出氢化钙与水反应的化学方程式
(2)现有875g氢化钙固体(含CaH296%),与足量水反应可生成多少克氢气?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)根据题中的叙述找出反应物、生成物书写方程式;
(2)首先列出方程式,根据题中的数据,列出比例关系进行求解.
(2)首先列出方程式,根据题中的数据,列出比例关系进行求解.
解答:解:(1)氢化钙和水反应生成氢氧化钙和氢气,化学方程式为:CaH2+2H2O=2H2↑+Ca(OH)2;
故答案为:CaH2+2H2O=2H2↑+Ca(OH)2;
(2)解:设875g氢化钙固体(含CaH296%)与足量水反应可生成氢气的质量为X
CaH2+2H2O═2H2↑+Ca(OH)2
42 4
875g×96% x
=
x=80g
答:875g氢化钙固体(含CaH296%)与足量水反应可生成氢气的质量为80g.
故答案为:CaH2+2H2O=2H2↑+Ca(OH)2;
(2)解:设875g氢化钙固体(含CaH296%)与足量水反应可生成氢气的质量为X
CaH2+2H2O═2H2↑+Ca(OH)2
42 4
875g×96% x
| 42 |
| 4 |
| 875g×96% |
| x |
x=80g
答:875g氢化钙固体(含CaH296%)与足量水反应可生成氢气的质量为80g.
点评:在解此类题时,首先根据题中的叙述书写方程式,然后根据方程式中的等量关系进行求解,需要注意代入方程式中的都是纯净物的质量.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在含有H2SO4和CuSO4溶液中加入一定量的铁粉,充分反应后,发现固体有剩余,则下面叙述正确的是( )
| A、溶液中一定有FeSO4 |
| B、溶液中一定有CuSO4 |
| C、固体物质中一定含有Cu |
| D、固体物质中一定不含有Fe |

 称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:
称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题: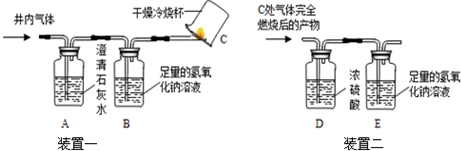
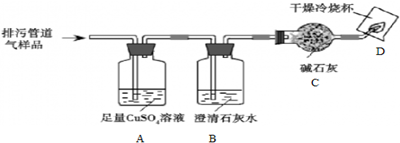
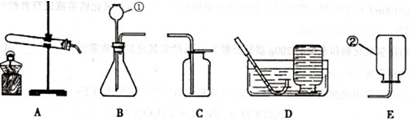
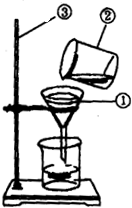 某学生为了使一杯浑浊的食盐水变成澄清透明,利用了如图所示的装置进行过滤.
某学生为了使一杯浑浊的食盐水变成澄清透明,利用了如图所示的装置进行过滤.