题目内容
10.以电石渣[主要成分Ca(OH)2和CaCO3]为原料制备KClO3的流程如图.
查阅资料:在75℃左右,氯化步骤中氯气转化成Ca(ClO3)2时发生一系列的反应,其中Cl2与Ca(OH)2反应的总化学方程式可表示为:
6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+aH2O
(1)氯化前,先将电石渣粉碎的目的是增大反应物的接触面积,加快反应速率.
(2)氯化步骤中所得产物氯酸钙Ca(ClO3)2中Cl的化合价为+5价,a数值为6.
(3)操作X为过滤.转化步骤中Ca(ClO3)2与KCl反应生成KClO3的化学方程式为Ca(ClO3)2+2KCl=2KClO3+CaCl2.(相关物质的溶解度见下表)
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| T℃时溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
【提出问题】滤渣M中除了电石渣原有的不溶性杂质外,还含有什么物质?
【猜想假设】①CaCO3; ②Ca(OH)2; ③CaCO3和Ca(OH)2.
【实验验证】
| 实验步骤 | 实验现象 | 结论 |
| 步骤1:取少量滤渣M加入盛水的小烧杯中,搅拌,静置后先加入几滴无色酚酞试液; | 观察到溶液变红色现象 | 猜想①不正确 |
| 步骤2:向小烧杯中继续加入足量的稀盐酸 | 观察到固体溶解并有气泡产生现象 | 猜想③正确 |
分析 (1)根据粉碎会增大反应物的接触面积加快反应速度进行分析;
(2)根据化合物中正负化合价代数和为零计算化合价.可以根据质量守恒定律前后原子个数不变来分析解答;
(3)根据过滤可以分离固液的混合物,结合反应物和复分解反应特点分析;
(4)根据物质的溶解性结合反应特点来分析解答;
解答 解:(1)依据影响化学反应速率的因素可知,反应物接触面积越大,反应越剧烈,黄铁矿粉碎的目的是:增大反应物的接触面积,加快反应速率;
故答案为:增大反应物的接触面积,加快反应速率;
(2)氯酸钙Ca(ClO3)2中钙的化合价为+2价,氧的化合价为-2价,设,氯的化合价为x,则(+2)+(x+(-2)×3)×2=0,x=+5;根据反应前后氧原子个数不变可知,a=(6×2)-(3×2)=6;
故答案为:+5;6;
(3)由图示可知,经过X操作后分离出了滤渣,故X是过滤;Ca(ClO3)2与KCl反应生成KClO3和CaCl2;
答案:过滤;Ca(ClO3)2+2KCl=2KClO3+CaCl2;
(4)滤渣M中除了电石渣原有的不溶性杂质外,还含有①CaCO3; ②Ca(OH)2;③CaCO3和Ca(OH)2的混合物;
步骤1的结论是猜想①不正确,说明含有Ca(OH)2;Ca(OH)2微溶于水,水溶液显碱性 能使酚酞变红色;故加入的是无色酚酞试液;
步骤2是猜想③正确;说明及含有碳酸钙又含有氢氧化钙;碳酸钙能溶于酸产生气体二氧化碳,故加入的试剂是稀盐酸;
答案:CaCO3和Ca(OH)2;几滴无色酚酞试液;溶液变红色;固体溶解并有气泡产生.
点评 本题为信息题的考查,解题的关键是利用题干中的信息结合相关知识对相关问题进行分析判断.

练习册系列答案
相关题目
4.除去下列物质中的少量杂质(括号内为杂质),所选试剂正确的是( )
| A. | CaCO3粉末(CaCl2粉末)--水 | B. | CaO粉末[Ca(OH)2粉末]--水 | ||
| C. | KCl溶液(KOH)--稀硝酸 | D. | NaOH溶液(Na2CO3)--稀盐酸 |
5. 在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.
在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.
探究一 M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:
①是Ca(OH)2,②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
探究二 过滤后澄清滤液中会有哪些溶质?
【提出猜想】猜想一:NaOH和Na2CO3;猜想二:NaOH和Ca(OH)2;猜想三:NaOH
(3)【实验验证】同学们针对“猜想一”进行了如下实验:
他们的实验结论是否正确?不正确,理由是溶液中氢氧化钠能与加入的少量盐酸反应,即使溶液中有Na2CO3溶液也可能不产生气体.
 在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.
在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.探究一 M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:
①是Ca(OH)2,②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量M溶液于 试管中,向其中滴加酚酞溶液. | 酚酞溶液变红色. | 猜想①正确,碳酸钠与其反应的化学 方程为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH. |
【提出猜想】猜想一:NaOH和Na2CO3;猜想二:NaOH和Ca(OH)2;猜想三:NaOH
(3)【实验验证】同学们针对“猜想一”进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入几滴稀盐酸 | 没有气体产生. | “猜想一”不成立 |
2.下列四种化肥样品中,分别加入熟石灰混合、研磨后能闻到刺激性气味的是( )
| A. | 硫酸钾 | B. | 磷矿粉 | C. | 氯化铵 | D. | 氯化钾 |
19.下列说法正确的是( )
| A. | 排水法收集氧气,要等导管口气泡均匀连续冒出时再开始收集 | |
| B. | 保持空气化学性质的最小粒子是空气分子 | |
| C. | 检验氢氧化钠与氯化铵反应生成的气体可用湿润的蓝色石蕊试纸 | |
| D. | 不同种元素最本质的区别是中子数不同 |
20.为验证Zn、Cu、Ag三种金属的活泼性顺序,下列试剂可以选用的是( )
| A. | ZnSO4溶液 | B. | 稀盐酸 | C. | AgNO3溶液 | D. | CuSO4溶液 |
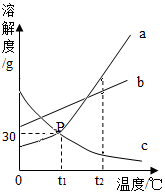 如图是a、b、c三种物质(不含结晶水)的溶解度曲线,a与c的溶解度曲线交于P点,请据图回答
如图是a、b、c三种物质(不含结晶水)的溶解度曲线,a与c的溶解度曲线交于P点,请据图回答