题目内容
18.为研究酸的性质,某研究小组进行了如下探究.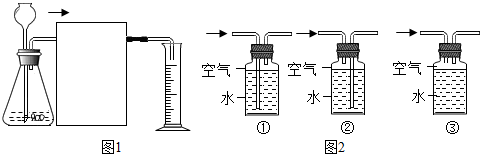
(1)小刚将颗粒大小相同的纯锌粒和粗锌粒分别加入相同浓度的稀硫酸中.写出锌与硫酸反应的化学方程式:Zn+H2SO4═ZnSO4+H2↑.
(2)小刚仔细观察后发现纯锌粒和硫酸的反应明显比粗锌粒慢.通过查阅资料小刚得知粗锌中含有一些不活泼金属.她猜想可能是粗锌中不活泼金属促进了锌和硫酸的反应.
为了验证小刚的猜想,你认为应该在盛有纯锌粒和稀硫酸的试管中,加入少量的下列哪种物质?B.
A.HCl B.CuCl2 C.NaCl D.CaCl2
(3)实验中小刚发现加入上述所选物质,纯锌和稀硫酸的反应都有不同程度的加快,请你分析可能的原因是什么?四种溶液中的Cl-对溶液起了促进作用.
(4)小刚想通过用一定质量粗锌和足量的硫酸反应,测量生成氢气的体积来计算粗锌的纯度.设计了如图1所示的实验装置.
在虚线框中应接入图2中的②,广口瓶上方残留的空气不会(填“会”或“不会”)对氢气体积的测量造成影响.
分析 (1)根据锌与硫酸反应生成硫酸锌和氢气,写出反应的化学方程式解答;
(2)根据金属活动性顺序解答;
(3)根据题中信息分析解答;
(4)根据氢气的密度比水的小解答.
解答 解:(1)锌粒与稀硫酸反应生成硫酸锌和氢气,反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑.
(2)由金属活动性顺序可知:钠、钙都比锌活泼,铜不如锌活泼,为了验证小刚的猜想,应该在盛有纯锌粒和稀硫酸的试管中,加入少量的CuCl2;
(3)实验中小刚发现加入上述所选物质,纯锌和稀硫酸的反应都有不同程度的加快,可能的原因是四种溶液中的Cl-对溶液起了促进作用;
(4)氢气的密度比水的小,收集氢气时应短进,故用一定质量粗锌和足量的硫酸反应,测量生成氢气的体积来计算粗锌的纯度设计了如图所示的实验装置.在虚线框中应接入图中的②,因为通过排出的水来测量氢气的体积,广口瓶上方残留的空气不会对氢气体积的测量造成影响.
故填:(1)Zn+H2SO4═ZnSO4+H2↑;(2)B;(3)四种溶液中的Cl-对溶液起了促进作用;(4)②;不会.
点评 本题主要考查化学实验的方案设计与评价,在解此类题时,首先分析题中考查的问题,然后结合所给的知识和学过的知识进行分析解答.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
2. 如图是硝酸钾和碳酸钾在不同温度时的溶解度曲线和溶解度数据表.
如图是硝酸钾和碳酸钾在不同温度时的溶解度曲线和溶解度数据表.
(1)根据表中的数据可知,图中的甲表示硝酸钾的溶解度曲线.
(2)在50℃时,将40g碳酸钾固体 溶解在50g水中,得到不饱和(填“饱和、不饱和”)溶液.
(3)若甲物质中混有少量的乙物质,提纯甲物质最好采取的方法是降温结晶(填”降温结晶或蒸发溶剂“).
(4)临近海边的人常常“夏天晒盐,冬天捞碱”,图中与“碱”的溶解度曲线相似的是碳酸钾.
(5)若将t1℃时的甲物质的饱和溶液200克和乙物质的饱和溶液200克分别升温到t2℃(不考虑水分蒸发)两物质的溶液中溶质的质量分数的关系是:甲小于乙(填大于、小于或等于).
(6)气体物质在水中的溶解能力与温度、压强两个因素.
 如图是硝酸钾和碳酸钾在不同温度时的溶解度曲线和溶解度数据表.
如图是硝酸钾和碳酸钾在不同温度时的溶解度曲线和溶解度数据表.| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 |
| K2CO3 | 110 | 114 | 121 | 126 | 139 | |
(2)在50℃时,将40g碳酸钾固体 溶解在50g水中,得到不饱和(填“饱和、不饱和”)溶液.
(3)若甲物质中混有少量的乙物质,提纯甲物质最好采取的方法是降温结晶(填”降温结晶或蒸发溶剂“).
(4)临近海边的人常常“夏天晒盐,冬天捞碱”,图中与“碱”的溶解度曲线相似的是碳酸钾.
(5)若将t1℃时的甲物质的饱和溶液200克和乙物质的饱和溶液200克分别升温到t2℃(不考虑水分蒸发)两物质的溶液中溶质的质量分数的关系是:甲小于乙(填大于、小于或等于).
(6)气体物质在水中的溶解能力与温度、压强两个因素.
3.化学小组同学取某黄铜(铜和锌的合金)样品进行如下实验,他们取该黄铜样品碎屑50g,把200g稀硫酸分4次加入到该样品中,测得数据记录如表:
(1)铜锌合金中铜的质量分数67.5%.
(2)当加入稀硫酸的质量为125g时,反应恰好完成.
(3)计算所用稀硫酸的浓度(写出计算过程).
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加人稀硫酸质量/g | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 43.5 | 37.0 | 33.75 | 33.75 |
(2)当加入稀硫酸的质量为125g时,反应恰好完成.
(3)计算所用稀硫酸的浓度(写出计算过程).
6.南京市国民经济和社会发展第“十二五”规划纲要指出,要做强做优电子信息等工业支柱产业.硅(Si)是信息技术的关键材料,常用以下方法制得纯硅,如图所示:

(1)图中①、③发生了置换反应,②发生了化合反应.写出②和③的化学反应方程式:
②Si+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4;③SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl.
(2)完成一种表示置换反应的通式:单质(I)+化合物(I)=单质(Ⅱ)+化合物(Ⅱ).
根据已学知识填表:

(1)图中①、③发生了置换反应,②发生了化合反应.写出②和③的化学反应方程式:
②Si+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4;③SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl.
(2)完成一种表示置换反应的通式:单质(I)+化合物(I)=单质(Ⅱ)+化合物(Ⅱ).
根据已学知识填表:
| 单质(I) | 单质(Ⅱ) | 相应的置换反应的化学方程式(各举一例) | |
| A | 金属 | 非金属 | |
| B | 金属(I) | 金属(Ⅱ) | |
| C | 非金属 | 金属 | |
| D | SiO2+2C$\frac{\underline{\;高温、电炉\;}}{\;}$Si+2CO↑ |
10.探究:学习小组利用如图装置探究温度对CO还原Fe2O3生成物的影响
查阅资料:CO2+Zn $\frac{\underline{\;\;△\;\;}}{\;}$CO+ZnO; FeCl3溶液遇KSCN溶液变红.
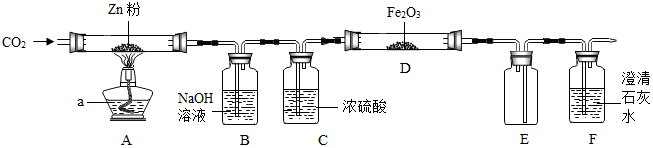
请回答下列问题:
(1)装置B的作用是吸收二氧化碳,发生的反应2NaOH+CO2═Na2CO3+H2O(化学方程式);某同学建议F后面应加一盏酒精灯,目的是把一氧化碳转化成二氧化碳.
(2)将研究小组分为两组,按如图装置进行对比实验:甲组用酒精灯、乙组用酒精喷灯对装置D进行加热,其产物均为黑色粉末(经检测为纯净物).两组分别用产物进行以下实验:
则甲组步骤1中反应的化学方程式是Fe3O4+8HCl=FeCl2+2FeCl3+4H2O,乙组得到的黑色粉末是铁.
(3)通过该对比实验结果,你可以归纳出温度不同,一氧化碳还原氧化铁的生成物不同结论.
查阅资料:CO2+Zn $\frac{\underline{\;\;△\;\;}}{\;}$CO+ZnO; FeCl3溶液遇KSCN溶液变红.

请回答下列问题:
(1)装置B的作用是吸收二氧化碳,发生的反应2NaOH+CO2═Na2CO3+H2O(化学方程式);某同学建议F后面应加一盏酒精灯,目的是把一氧化碳转化成二氧化碳.
(2)将研究小组分为两组,按如图装置进行对比实验:甲组用酒精灯、乙组用酒精喷灯对装置D进行加热,其产物均为黑色粉末(经检测为纯净物).两组分别用产物进行以下实验:
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入盐酸 | 溶解,无气泡,溶液呈浅黄绿色(含两种金属离子) | 溶解,有气泡,溶液呈浅绿色 |
| 2 | 取步骤1所得溶液,滴加KSCN溶液 | 变红 | 无现象 |
(3)通过该对比实验结果,你可以归纳出温度不同,一氧化碳还原氧化铁的生成物不同结论.
7. 研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧缺有明亮的火焰.该小组同学进行了如下探究:
研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧缺有明亮的火焰.该小组同学进行了如下探究:
①写出铁丝在氧气中燃烧的化学方程式:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4-
②探究一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图).由此可知:蜡烛燃烧产生的火焰是由气态(填“固态”或“气态”)物质燃烧形成的.
③探究二:物质燃烧产生火焰的根本原因是什么?
查阅资料
由表可知:物质燃烧能否产生火焰与其沸点(填“熔点”或“沸点”)和燃烧时温度有关.由此推测:钠在燃烧时,有(填“有”或“没有”)火焰产生.
④木炭在氧气中燃烧没有火焰,其原因可能是燃烧时的温度低于沸点.
 研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧缺有明亮的火焰.该小组同学进行了如下探究:
研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧缺有明亮的火焰.该小组同学进行了如下探究:①写出铁丝在氧气中燃烧的化学方程式:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4-
②探究一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图).由此可知:蜡烛燃烧产生的火焰是由气态(填“固态”或“气态”)物质燃烧形成的.
③探究二:物质燃烧产生火焰的根本原因是什么?
查阅资料
| 物质 | 熔点╱℃ | 沸点╱℃ | 燃烧时温度╱℃ |
| 石蜡 | 50-70 | 300-550 | 约600 |
| 铁 | 1535 | 2750 | 约1800 |
| 钠 | 97.8 | 883 | 约1400 |
④木炭在氧气中燃烧没有火焰,其原因可能是燃烧时的温度低于沸点.
 物质之间发生化学反应时常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某班同学为证明NaOH能与稀盐酸发生中和反应,从不同角度设计了如下实验方案,并进行实验.
物质之间发生化学反应时常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某班同学为证明NaOH能与稀盐酸发生中和反应,从不同角度设计了如下实验方案,并进行实验.
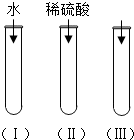 氧化铜(CuO)是一种黑色固体,可溶于稀硫酸中.某同学想知道是稀硫酸中的H2O、H+和SO42-中的哪种粒子能使氧化铜溶解.请你和他一起通过如图所示三个实验来完成这次探究活动
氧化铜(CuO)是一种黑色固体,可溶于稀硫酸中.某同学想知道是稀硫酸中的H2O、H+和SO42-中的哪种粒子能使氧化铜溶解.请你和他一起通过如图所示三个实验来完成这次探究活动