题目内容
8.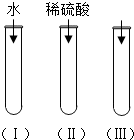 氧化铜(CuO)是一种黑色固体,可溶于稀硫酸中.某同学想知道是稀硫酸中的H2O、H+和SO42-中的哪种粒子能使氧化铜溶解.请你和他一起通过如图所示三个实验来完成这次探究活动
氧化铜(CuO)是一种黑色固体,可溶于稀硫酸中.某同学想知道是稀硫酸中的H2O、H+和SO42-中的哪种粒子能使氧化铜溶解.请你和他一起通过如图所示三个实验来完成这次探究活动(1)你提出的假设是可能是H+使CuO溶解;
(2)通过实验(Ⅰ)可以证明水分子不能使氧化铜溶解;
(3)要证明另外两种粒子能否溶解氧化铜,还需要进行实验(Ⅱ)和(Ⅲ),在(Ⅲ)中应该加入Na2SO4溶液,实验中观察到的实验现象为固体不溶解;
(4)探究结果为稀硫酸中的H+使CuO溶解.
分析 (1)稀硫酸中存在三种粒子,即水分子、氢离子、硫酸根离子,据此进行分析解答;
(2)实验I中加入的是水,实验I是验证水能否使氧化铜溶解;
(3)实验I、实验III中的氧化铜不溶解,II中氧化铜溶解,据此进行分析解答;
(4)根据分析得出结论.
解答 解:(1)稀硫酸中存在水分子、氢离子、硫酸根离子,可能是稀硫酸中的水分子、氢离子或硫酸根离子中的一种使氧化铜溶解;故答案为:可能是H+使CuO溶解;
(2)实验I中,氧化铜不溶解,说明水分子不能使氧化铜溶解;故填:水分子不能使氧化铜溶解;
(3)因为Ⅰ实验证明了H2O不能使CuO溶解的结论,实验Ⅱ中既有H+,又有SO42-和H2O,其中水分子已经证明了不能使CuO溶解,而且知道实验Ⅱ中的现象是氧化铜溶解,但三个实验必须得出实验结果,如果实验三再加盐酸,那硫酸根就没法证明了,所以实验Ⅲ中应加入的物质应该是含硫酸根的溶液;故填:Na2SO4等液;固体不溶解;
(4)通过实验可以得知,水分子和硫酸根离子都不能使氧化铜溶解,使氧化铜溶解的是氢离子,只有含有大量氢离子的溶液才可以和氧化铜反应,使之溶解;故填:稀硫酸中的H+使CuO溶解.
点评 本题主要考查了酸溶液和氧化铜反应的本质,是溶液中的氢离子和氧化铜反应的结果,培养学生分析问题、解决问题的能力.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
3.某兴趣小组同学用大理石和盐酸反应制取二氧化碳,将制得的气体通入澄清石灰水,观察到石灰水未变浑浊,他们对此现象产生了好奇.同学们提出了下列三个假设:
假设①:石灰水已变质;假设②:制得的气体中无二氧化碳;假设③:制得的气体中有一定量的氯化氢气体.
(1)同学们先探究假设①是否成立.他们将适量的原试剂瓶中的澄清的石灰水倒入小试管中,然后通入二氧化碳气体(填写实验操作),他们根据实验现象确认了石灰水未变质.他们接着探究,通过实验否定了假设②.
(2)同学们继续设计了两个实验来探究假设③,如表所示:
上述实验一中的A物质是硝酸银溶液,实验二中的实验现象是产生气泡
(3)同学们通过实验确定了澄清石灰水未变浑浊的原因是制得的气体中含有一定量的氯化氢气体.请解释将制得的气体通入澄清石灰水后,石灰水不变浑浊的原因是稀盐酸和氢氧化钙反应生成了氯化钙和水.
假设①:石灰水已变质;假设②:制得的气体中无二氧化碳;假设③:制得的气体中有一定量的氯化氢气体.
(1)同学们先探究假设①是否成立.他们将适量的原试剂瓶中的澄清的石灰水倒入小试管中,然后通入二氧化碳气体(填写实验操作),他们根据实验现象确认了石灰水未变质.他们接着探究,通过实验否定了假设②.
(2)同学们继续设计了两个实验来探究假设③,如表所示:
| 实验操作 | 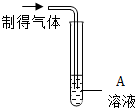 | 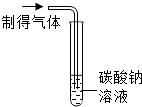 |
| 实验现象 | 出现白色沉淀 | ? |
| 实验结论 | 制得的气体中有氯化氢气体 | 制得的气体中有氯化氢气体 |
(3)同学们通过实验确定了澄清石灰水未变浑浊的原因是制得的气体中含有一定量的氯化氢气体.请解释将制得的气体通入澄清石灰水后,石灰水不变浑浊的原因是稀盐酸和氢氧化钙反应生成了氯化钙和水.
13. C02与NaOH溶液能发生反应,但看不到明显现象.某化学兴趣小组为验证CO2与NaOH溶液发生了反应,进行如下探究活动.
C02与NaOH溶液能发生反应,但看不到明显现象.某化学兴趣小组为验证CO2与NaOH溶液发生了反应,进行如下探究活动.
【查阅资料】
(1)CO2与NaOH反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.
【设计实验】
(2)方案一:
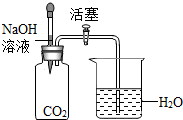
(3)方案二:接如图所示装置进行实验.
【反思与评价】
(4)有同学认为方案二根据实验现象不能得出“CO2与NaOH溶液发生了反应”的结论,还应再做对比实验,理由是二氧化碳可以溶于水.
 C02与NaOH溶液能发生反应,但看不到明显现象.某化学兴趣小组为验证CO2与NaOH溶液发生了反应,进行如下探究活动.
C02与NaOH溶液能发生反应,但看不到明显现象.某化学兴趣小组为验证CO2与NaOH溶液发生了反应,进行如下探究活动.【查阅资料】
(1)CO2与NaOH反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.
【设计实验】
(2)方案一:
| 实验操作 | 实验现象 | 结论 |
| 往盛有NaOH溶液的试管中通人CO2,然后滴人足量的氯化钙溶液 | 产生了沉淀 | CO2与NaOH溶液发生了反应 |
| 1实验操作 | 实验现象 | 结论 |
| 将氢氧化钠溶液滴入广口瓶中,然后打开活塞 | 烧杯中的水吸入集气瓶中 | CO2与NaOH溶液发生了反应 |
(4)有同学认为方案二根据实验现象不能得出“CO2与NaOH溶液发生了反应”的结论,还应再做对比实验,理由是二氧化碳可以溶于水.
20.下列归纳和总结完全正确的一组是( )
| A.对安全的认识 | B.用“化学”眼光分析 |
| ①点燃可燃性气体前一定要验纯 ②煤气泄漏立即打开排气扇 ③煤矿矿井要保持通风、严禁烟火 | ①洗涤剂去除油污是因为乳化作用 ②用适量的熟石灰可中和土壤的酸性 ③用水灭火是降低温度至可燃物的着火点以下 |
| C.化学与健康 | D.对除杂和鉴别的认识 |
| ①霉变的大米洗净烧熟后可以食用 ②利用甲醛水溶液浸泡水产品防腐 ③人体缺铁会导致贫血 | ①用灼热的CuO除去CO中少量CO2 ②用Ca(OH)2溶液除去NaOH溶液中的Na2CO3 ③用燃烧的方法区分羊毛和涤纶 |
| A. | A | B. | B | C. | C | D. | D |
17.日常生活中的下列物质,属于纯净物的是( )
| A. | 糖水 | B. | 牛奶 | C. | 氮气 | D. | 洁净的空气 |