题目内容
1.用正确化学用语填空:(1)地壳中含量居第二位的元素Si;(2)保持氯化氢化学性质的最小的粒子HCl;
(3)氯化亚铁溶液中大量存在的阳离子Fe2+;(4)硫酸铝中铝元素的化合价$\stackrel{+3}{Al}$2(SO4)3.
分析 (1)地壳中含量居第二位的元素是硅元素,写出其元素符号即可.
(2)由分子构成的物质,分子是保持物质化学性质的最小粒子,据此进行分析解答.
(3)氯化亚铁溶液中大量存在的阳离子是亚铁离子.
(4)硫酸铝中铝元素显+3价;化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后.
解答 解:(1)地壳中含量居第二位的元素是硅元素,其元素符号为:Si.
(2)氯化氢是由氯化氢分子构成的,保持氯化氢化学性质的最小的粒子是氯化氢分子,其分子符号为:HCl.
(3)氯化亚铁溶液中大量存在的阳离子是亚铁离子,其离子符号为:Fe2+.
(4)硫酸铝中铝元素显+3价;化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,硫酸铝中铝元素的化合价可表示为:.
故答案为:(1)Si;(2)HCl;(3)Fe2+;(4)$\stackrel{+3}{Al}$2(SO4)3.
点评 本题难度不大,掌握常见化学用语(元素符号、分子符号、化合价、离子符号等)的书写方法、离子符号与化合价表示方法的区别等是正确解答此类题的关键.

练习册系列答案
相关题目
11.有铁粉和铜粉的均匀混合物,甲、乙、丙三位同学分别取该混合物与稀硫酸反应,所得数据如表所示:
请分析数据,回答下列问题:
(1)10g混合物中所含铁粉的质量6g.
(2)稀硫酸中溶质质量分数为多少?(列式计算,写出相关的文字和计算过程)
(3)若取用金属混合物15g,加入120g稀硫酸中,充分反应后所得溶液中溶质的质量为22.8g.
| 甲 | 乙 | 丙 | |
| 取用金属混合物的质量 | 10 | 10 | 20 |
| 取用稀硫酸的质量/g | 100 | 200 | 100 |
| 反应后过滤,得干燥固体的质量/g | 4 | 4 | 13 |
(1)10g混合物中所含铁粉的质量6g.
(2)稀硫酸中溶质质量分数为多少?(列式计算,写出相关的文字和计算过程)
(3)若取用金属混合物15g,加入120g稀硫酸中,充分反应后所得溶液中溶质的质量为22.8g.
9.加水溶解后能形成溶液的是( )
| A. | 泥沙 | B. | 氯化银 | C. | 食用油 | D. | 蔗糖 |
16.向硝酸银和硝酸铜的混合溶液中加入一定量的锌粉.充分反应后过滤,往滤液中滴加盐酸,有白色沉淀生成.下列说法中正确的是( )
| A. | 所得溶液中可能含有Cu2+ | |
| B. | 所得滤渣中可能含有铜和锌 | |
| C. | 所得滤液中一定含有Ag+、Zn2+、Cu2+ | |
| D. | 所得滤渣中一定含有银和铜 |
6.现有23g久置的生石灰,测得其中钙元素与碳元素的质量比为10:1,在室温下,将该混合物与100g稀盐酸混合,恰好完全反应,所得的不饱和溶液的质量为118.6g,则原混合物中钙元素的质量为( )
| A. | 2.7g | B. | 12g | C. | 12.4g | D. | 16.4g |
10.下列食物中富含蛋白质的是( )
| A. | 西瓜 | B. | 鲫鱼 | C. | 花生油 | D. | 马铃薯 |
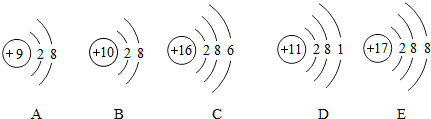
 化学是研究物质的组成、结构,性质及其变化规律的基础自然科学,请回答下列问题:
化学是研究物质的组成、结构,性质及其变化规律的基础自然科学,请回答下列问题: