题目内容
20.过氧化钠(Na2O2)可用作呼吸面具的供氧剂.实验室有一瓶放置较长时间的过氧化钠样品,某研究小组对其成分和性质进行了如下探究.【查阅资料】过氧化钠能与空气中水和二氧化碳反应生成氧气:
2Na2O2+2H2O=4NaOH+O2↑,2Na2O2+2CO2═2Na2CO3+O2.
【提出问题】过氧化钠是否变质?
【猜想与假设】假设1:过氧化钠未变质;
假设2:过氧化钠部分变质;
假设3:过氧化钠全部变质.
【实验探究】
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 取部分固体于试管中,加人足量的水,在试管口播人带火星的木条; | 固体完全溶解, 木条复然 | 假设3 不成立 |
| ② | 取少量①中溶液于试管中,滴加足量的稀盐酸,振荡. | 有气泡生成 | 假设2成立 |
【实验探究】实验③:取少量①中溶液于试管中,加人足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液变红.
【定性分析】(1)由实验③可以确定①中溶液含有的溶质是Na2CO3、NaOH(填化学式);实验③中所发生的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl
(2)小明认为,由上述实验无法确定原固体样品中是否含有氢氧化钠,理由是过氧化钠和水反应也能生成氢氧化钠.
【反思与提高】过氧化钠长期暴露在空气中,最终会变质为Na2CO3(填化学式)
分析 【猜想与假设】根据气体的检验方法可知是氧气,根据有气泡产生,说明含有碳酸钠;
【定性分析】(1)根据加入足量的氯化钙溶液,有白色沉淀生成,说明含有碳酸钠;静置,向上层清液中滴加2滴无色酚酞试液,溶液变红,说明含有氢氧化钠解答;
(2)根据过氧化钠与水反应能生成氢氧化钠,可推出结论是否正确;
【反思提高】根据过氧化钠易与二氧化碳反应产生碳酸钠解答.
解答 解:【猜想与假设】①取部分固体于试管中,加入适量的水,在试管口插入带火星的木条,固体完全溶解,木条复燃,可知是氧气,故假设3不正确;
②取少量①中溶液于试管中,滴加足量的稀盐酸,有气泡生成,说明含有碳酸钠;
【定性分析】(1)加入足量的氯化钙溶液,有白色沉淀生成,说明含有碳酸钠;静置,向上层清液中滴加2滴无色酚酞试液,溶液变红,说明含有氢氧化钠,以确定①中溶液含有的溶质是NaOH、Na2CO3;碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,反应的化学方程式为:Na2CO3+CaCl2=2NaCl+CaCO3↓;
(2)滤液中滴加无色酚酞试液,若液体变红,不能证明原粉末中有NaOH,因为过氧化钠与水反应能生成氢氧化钠,不能说明原来是否存在.
【反思提高】过氧化钠易与二氧化碳反应,还能和水反应变质,最终转化为Na2CO3;
故答案为:【实验探究】
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 取部分固体于试管中,加人足量的水,在试管口插人带火星的木条; | 固体完全溶解, 木条复然 | 假设__3__ 不成立 |
| ② | 取少量①中溶液于试管中,滴加足量的稀盐酸,振荡. | 有气泡生成 | 假设2成立 |
(2)过氧化钠和水反应也能生成氢氧化钠;
【反思与提高】Na2CO3.
点评 该考点的命题方向主要是以实验探究题的形式,给出有关的信息提示和相关数据,让学生通过实验探究,分析推断出该物质的组成成分;中考的重点是考查学生通过实验的方法来研究物质的组成成分以及含量能力.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
11.下列描述错误的是( )
| A. | 化学变化中原子是最小的粒子 | |
| B. | 化学反应的本质是分子的破裂,原子的重新组合 | |
| C. | 分子是由原子构成的 | |
| D. | 分子可以再分,而原子不可再分 |
5.对有关物质的应用,其中叙述错误的是( )
| A. | 氧气用于食品保鲜 | B. | 氦气充飞艇 | ||
| C. | 氮气用于制化肥 | D. | 石墨做汽车电刷 |
12.下列说法不正确的是( )
| A. | 木炭在氧气中剧烈燃烧,生成黑色固体 | |
| B. | 铁丝在氧气中燃烧,火星四射 | |
| C. | 红磷在空气中燃烧,产生大量的白烟 | |
| D. | 硫在空气中燃烧,生成有刺激性气味气体 |
9.用括号内的物质或方法除去下列各组中的杂质,其中错误的是( )
| A. | 氢氧化钠溶液中混有少量的碳酸钠(适量的氢氧化钙溶液) | |
| B. | 铜粉中混有铁粉(用磁铁吸引) | |
| C. | 氧化钙中混有少量的碳酸钙(适量盐酸) | |
| D. | 二氧化碳混有少量的一氧化碳(灼热的氧化铜) |
10.下列实验操作错误的是( )
| A. |  细铁丝燃烧 | B. |  稀释浓硫酸 | C. |  过滤 | D. |  加入少量液体 |
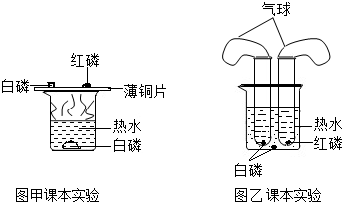 小明与同学一起对教材中“燃烧的条件”这个实验(图甲)进行了如下改进(图乙):去掉铜片,将足量的红磷和白磷分别放在两个大试管中,在试管口各自套一个气球,用线固定,然后将两支大使馆同时浸在盛有热水的烧杯中
小明与同学一起对教材中“燃烧的条件”这个实验(图甲)进行了如下改进(图乙):去掉铜片,将足量的红磷和白磷分别放在两个大试管中,在试管口各自套一个气球,用线固定,然后将两支大使馆同时浸在盛有热水的烧杯中