题目内容
9.用括号内的物质或方法除去下列各组中的杂质,其中错误的是( )| A. | 氢氧化钠溶液中混有少量的碳酸钠(适量的氢氧化钙溶液) | |
| B. | 铜粉中混有铁粉(用磁铁吸引) | |
| C. | 氧化钙中混有少量的碳酸钙(适量盐酸) | |
| D. | 二氧化碳混有少量的一氧化碳(灼热的氧化铜) |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、碳酸钠能与适量的氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、铁粉能被磁铁吸引,而铜粉不能,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
C、氧化钙和碳酸钙均能与盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
D、一氧化碳能与灼热的氧化铜反应生成铜和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:C.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
20.过氧化钠(Na2O2)可用作呼吸面具的供氧剂.实验室有一瓶放置较长时间的过氧化钠样品,某研究小组对其成分和性质进行了如下探究.
【查阅资料】过氧化钠能与空气中水和二氧化碳反应生成氧气:
2Na2O2+2H2O=4NaOH+O2↑,2Na2O2+2CO2═2Na2CO3+O2.
【提出问题】过氧化钠是否变质?
【猜想与假设】假设1:过氧化钠未变质;
假设2:过氧化钠部分变质;
假设3:过氧化钠全部变质.
【实验探究】
【提出新问题】部分变质的过氧化钠中是否含有氢氧化钠?
【实验探究】实验③:取少量①中溶液于试管中,加人足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液变红.
【定性分析】(1)由实验③可以确定①中溶液含有的溶质是Na2CO3、NaOH(填化学式);实验③中所发生的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl
(2)小明认为,由上述实验无法确定原固体样品中是否含有氢氧化钠,理由是过氧化钠和水反应也能生成氢氧化钠.
【反思与提高】过氧化钠长期暴露在空气中,最终会变质为Na2CO3(填化学式)
【查阅资料】过氧化钠能与空气中水和二氧化碳反应生成氧气:
2Na2O2+2H2O=4NaOH+O2↑,2Na2O2+2CO2═2Na2CO3+O2.
【提出问题】过氧化钠是否变质?
【猜想与假设】假设1:过氧化钠未变质;
假设2:过氧化钠部分变质;
假设3:过氧化钠全部变质.
【实验探究】
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 取部分固体于试管中,加人足量的水,在试管口播人带火星的木条; | 固体完全溶解, 木条复然 | 假设3 不成立 |
| ② | 取少量①中溶液于试管中,滴加足量的稀盐酸,振荡. | 有气泡生成 | 假设2成立 |
【实验探究】实验③:取少量①中溶液于试管中,加人足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液变红.
【定性分析】(1)由实验③可以确定①中溶液含有的溶质是Na2CO3、NaOH(填化学式);实验③中所发生的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl
(2)小明认为,由上述实验无法确定原固体样品中是否含有氢氧化钠,理由是过氧化钠和水反应也能生成氢氧化钠.
【反思与提高】过氧化钠长期暴露在空气中,最终会变质为Na2CO3(填化学式)
4.甲、乙、丙三种固体物质的溶解度曲线如图所示,下列说法正确的是( )

| A. | 若甲固体中含有少量乙,可用降温结晶的方法提纯甲 | |
| B. | 三种物质的溶解度都随温度的升高而增大 | |
| C. | 将35℃时丙的饱和溶液降温到25℃,其溶液的溶质质量分数变小 | |
| D. | 25℃时,甲物质饱和溶液的溶质质量分数为30% |
14.配制100g 2%的NaOH溶液,下列操作正确的是( )
| A. | 用托盘天平称取2.0gNaOH固体时,需在左、右两盘各放一张质量相等的纸 | |
| B. | 用500mL规格的量筒量取98.0mL水 | |
| C. | 将称取的NaOH固体倒入量筒中溶解 | |
| D. | 溶解时要用玻璃棒不断搅拌 |
1.物质的性质决定它的用途.下列物质的性质与用途对应关系不正确的( )
| A. | 食醋具有酸性,可用于消除松花蛋中所含碱性物质的涩味 | |
| B. | 铁的活泼性比铝弱,铁制品比铝制品在空气中更耐腐蚀 | |
| C. | 磷燃烧能产生白烟,可用于制作烟幕弹 | |
| D. | 糖类氧化可以放出能量--做人类供能的食物 |
18.下列常用化学仪器可用于配制溶液、加热较多量液体、作反应容器的是( )
| A. | 烧杯 | B. | 试管 | C. | 量筒 | D. | 滴管 |
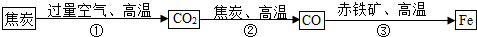
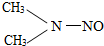 2013年震惊全国的复旦大学投毒案,使用剧毒化学物质N-二甲基亚硝胺(模型见图)该化学物质常温下呈黄色液体,中性,有弱臭味,粘滞度低,溶于水、乙醇、乙醚、二氯甲烷.侵入途径:摄入、吸入或经皮肤吸收,引起肝、肾损害甚至死亡.危险特性:遇明火、高热易燃.与强氧化剂可发生反应,受热分解放出有毒的一氧化氮烟气,还生成两种常见的碳氧化合物.
2013年震惊全国的复旦大学投毒案,使用剧毒化学物质N-二甲基亚硝胺(模型见图)该化学物质常温下呈黄色液体,中性,有弱臭味,粘滞度低,溶于水、乙醇、乙醚、二氯甲烷.侵入途径:摄入、吸入或经皮肤吸收,引起肝、肾损害甚至死亡.危险特性:遇明火、高热易燃.与强氧化剂可发生反应,受热分解放出有毒的一氧化氮烟气,还生成两种常见的碳氧化合物.