题目内容
8.如图为粗盐的提纯过程,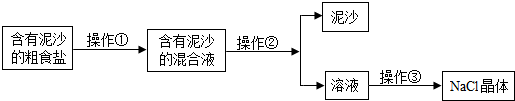
(1)其中操作①、③依次为溶解、蒸发;操作②玻璃棒的作用是引流.
(2)若NaCl的产率偏低(产率=$\frac{所得晶体的质量}{所取样品的质量}$),则可能的原因是(填字母)BC.
A.过滤时滤纸有破损 B.蒸发时有固体溅出 C.溶解含泥沙的粗食盐时,加入的水量不足
(3)用上述实验所得NaCl晶体配制50g溶质质量分数为5%NaCl溶液,配制时需要的玻璃仪器有烧杯、玻璃棒、滴管、量筒.
分析 (1)粗盐提纯过程中,操作顺序为:溶解、过滤、蒸发;
玻璃棒的用途有搅拌、引流、转移物质等;
(2)过滤时滤纸有破损,会导致不溶于水的固体进入滤液中;
蒸发时有固体溅出,会导致氯化钠的损失;
溶解含泥沙的粗食盐时,加入的水量不足,会导致氯化钠不能完全溶解;
(3)配制一定质量分数的溶液时,需要用量筒量取液体.
解答 解:(1)其中操作①、③依次为溶解、蒸发;
操作②玻璃棒的作用是引流.
故填:溶解;蒸发;引流.
(2)A.过滤时滤纸有破损,会导致不溶于水的固体进入滤液中,从而导致氯化钠质量偏大,进一步会导致NaCl的产率偏高;
B.蒸发时有固体溅出,会导致氯化钠的损失,从而导致NaCl的产率偏低;
C.溶解含泥沙的粗食盐时,加入的水量不足,会导致氯化钠不能完全溶解,从而导致氯化钠质量偏小,从而导致NaCl的产率偏低.
故填:BC.
(3)配制时需要的玻璃仪器有烧杯、玻璃棒、滴管、量筒.
故填:量筒.
点评 溶解时,利用玻璃棒搅拌可以加快溶解速率,蒸发时利用玻璃棒搅拌可以防止液体飞溅,要注意理解.

练习册系列答案
相关题目
13.下列实验现象描述不正确的是( )
| A. | 电解水时正极产生的气体比负极产生的气体多 | |
| B. | 硫在空气中燃烧,产生淡蓝色火焰 | |
| C. | 细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 铜绿受热分解,固体由绿色变为黑色 |
20.过氧化钠(Na2O2)可用作呼吸面具的供氧剂.实验室有一瓶放置较长时间的过氧化钠样品,某研究小组对其成分和性质进行了如下探究.
【查阅资料】过氧化钠能与空气中水和二氧化碳反应生成氧气:
2Na2O2+2H2O=4NaOH+O2↑,2Na2O2+2CO2═2Na2CO3+O2.
【提出问题】过氧化钠是否变质?
【猜想与假设】假设1:过氧化钠未变质;
假设2:过氧化钠部分变质;
假设3:过氧化钠全部变质.
【实验探究】
【提出新问题】部分变质的过氧化钠中是否含有氢氧化钠?
【实验探究】实验③:取少量①中溶液于试管中,加人足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液变红.
【定性分析】(1)由实验③可以确定①中溶液含有的溶质是Na2CO3、NaOH(填化学式);实验③中所发生的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl
(2)小明认为,由上述实验无法确定原固体样品中是否含有氢氧化钠,理由是过氧化钠和水反应也能生成氢氧化钠.
【反思与提高】过氧化钠长期暴露在空气中,最终会变质为Na2CO3(填化学式)
【查阅资料】过氧化钠能与空气中水和二氧化碳反应生成氧气:
2Na2O2+2H2O=4NaOH+O2↑,2Na2O2+2CO2═2Na2CO3+O2.
【提出问题】过氧化钠是否变质?
【猜想与假设】假设1:过氧化钠未变质;
假设2:过氧化钠部分变质;
假设3:过氧化钠全部变质.
【实验探究】
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 取部分固体于试管中,加人足量的水,在试管口播人带火星的木条; | 固体完全溶解, 木条复然 | 假设3 不成立 |
| ② | 取少量①中溶液于试管中,滴加足量的稀盐酸,振荡. | 有气泡生成 | 假设2成立 |
【实验探究】实验③:取少量①中溶液于试管中,加人足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液变红.
【定性分析】(1)由实验③可以确定①中溶液含有的溶质是Na2CO3、NaOH(填化学式);实验③中所发生的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl
(2)小明认为,由上述实验无法确定原固体样品中是否含有氢氧化钠,理由是过氧化钠和水反应也能生成氢氧化钠.
【反思与提高】过氧化钠长期暴露在空气中,最终会变质为Na2CO3(填化学式)
18.下列常用化学仪器可用于配制溶液、加热较多量液体、作反应容器的是( )
| A. | 烧杯 | B. | 试管 | C. | 量筒 | D. | 滴管 |