题目内容
15.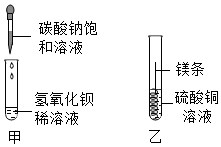 某同学进行如图两个实验:
某同学进行如图两个实验:(l)甲实验中反应的化学方程式为Ba(OH)2+Na2CO3═BaCO3↓+2NaOH;
(2)乙实验观察到的现象是镁条表面出现红色固体,溶液由蓝色变成无色
(3)把甲、乙反应后的溶液倒入同一烧杯,发现有白色沉淀生成.他决定对白色沉淀的成分进行探究.
【查阅资料】硫酸钡不溶于酸.
【提出猜想】白色沉淀为:Ⅰ.Mg(OH)2;Ⅱ.Mg(OH)2和BaSO4;Ⅲ.Mg(OH)2和MgCO3.
【实验方案】
| 实验操作 | 实验现象与结论 |
| 过滤、洗涤白色沉淀备用;向白色沉淀中加入盐酸至过量 | ①若沉淀全部溶解,且无其它现象;猜想Ⅰ成立;其化学反应方程式为Mg(OH)2+2HCl=MgCl2+2H2O. ②若白色沉淀部分溶解且无气体产生,猜想Ⅱ成立. ③若沉淀完全溶解,且有气体产生,猜想Ⅲ成立. |
分析 (1)根据碳酸钠与氢氧化钡反应生成碳酸钡沉淀和氢氧化钠解答;
(2)根据金属活动性顺序,镁可以把铜从其盐溶液中置换出来解答;
(3)根据甲、乙反应后的溶液倒入同一烧杯,发现有白色沉淀生成,由反应的量分析滤液的溶质成分;
【实验方案】根据氢氧化镁能与盐酸反应;硫酸钡不溶于酸,碳酸镁与盐酸反应生成二氧化碳气体设计实验.
【拓展与思考】根据物质的性质及反应后的溶液中碳酸钠与氢氧化钡不能共存解答.
解答 解:
(1)甲实验中是:碳酸钠与氢氧化钡反应生成碳酸钡沉淀和氢氧化钠,反应的化学方程式为Ba(OH)2+Na2CO3═BaCO3↓+2NaOH;
(2)金属活动性顺序,镁可以把铜从其盐溶液中置换出来,镁与硫酸铜反应,生成铜与硫酸镁,乙实验观察到的现象是:镁条表面出现红色固体,溶液由蓝色变成无色.
(3)
【提出猜想】甲、乙反应后的溶液倒入同一烧杯,发现有白色沉淀生成,说明乙中硫酸镁与甲中的氢氧化钡、碳酸钠或氢氧化钠反应,生成氢氧化镁沉淀、碳酸镁沉淀或硫酸钡沉淀;
如果甲中碳酸钠与氢氧化钡恰好完全反应,则硫酸镁与甲中的氢氧化钠反应,生成氢氧化镁沉淀,白色沉淀为:Ⅰ.Mg(OH)2;
如果氢氧化钡有剩余,则白色沉淀为:Ⅱ.Mg(OH)2和BaSO4;
如果碳酸钠有剩余,则白色沉淀为:Ⅲ.Mg(OH)2和MgCO3.
【实验方案】根据氢氧化镁能与盐酸反应;硫酸钡不溶于酸,碳酸镁与盐酸反应生成二氧化碳气体设计实验如下:
| 实验操作 | 实验现象与结论 |
| 过滤、洗涤白色沉淀备用;向白色沉淀中加入盐酸至过量 | ①若沉淀全部溶解,且无其它现象;猜想Ⅰ成立;其化学反应方程式为 Mg(OH)2+2HCl=MgCl2+2H2O. ②若 白色沉淀部分溶解且无气体产生,猜想Ⅱ成立. ③若沉淀完全溶解,且有气体产生,猜想Ⅲ成立. |
答案:
(1)Ba(OH)2+Na2CO3═BaCO3↓+2NaOH;
(2)镁条表面出现红色固体;
(3)【提出猜想】Mg(OH)2;
【实验方案】
| 实验操作 | 实验现象与结论 |
| 过滤、洗涤白色沉淀备用;向白色沉淀中加入盐酸至过量 | ①若沉淀全部溶解,且无其它现象;猜想Ⅰ成立;其化学反应方程式为 Mg(OH)2+2HCl=MgCl2+2H2O. ②若 白色沉淀部分溶解且无气体产生,猜想Ⅱ成立. ③若沉淀完全溶解,且有气体产生,猜想Ⅲ成立. |
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
5.只需要一次实验就能将H2SO4、NaCl、NaOH三种无色溶液区别开来的是( )
| A. | 纯碱溶液 | B. | 稀盐酸 | C. | pH试纸 | D. | 酚酞试液 |
6.豆腐脑是一道著名的中式传统小吃,更受沈阳人的喜爱.各地口味不同;北方多爱咸食,而南方则偏爱甜味,亦有地区喜爱麻辣.豆腐脑是煮熟的热豆浆与凝固剂接触导致大豆蛋白溶胶发生的蛋白质聚沉,目前市场有使用硫酸钙或葡萄糖作豆浆凝固剂.请设计实验方案来区分硫酸钙和葡萄糖两种物质.
| 实验方案 | 观察现象 | |
| 葡萄糖 | 硫酸钙 | |
| ①取样品,灼烧 | 可以燃烧 | 不能燃烧 |
| ②取样品,溶解,加入氯化钡 | 没有明显现象 | 有白色沉淀生成 |
| ③取样品,溶解,加入氢氧化钡 | 没有明显现象 | 有白色沉淀生成 |
| ④取样品,溶解,加入硝酸钡 | 没有明显现象 | 有白色沉淀生成 |
10.下列叙述正确的是( )
| A. | 由同种分子构成的物质不一定是纯净物 | |
| B. | 铁制金属防盗门上的锈可以阻止防盗门再生锈 | |
| C. | 湖水经沉淀、过滤、吸附等净化处理后,即可得纯水 | |
| D. | 热塑性塑料和热固性塑料可以通过加热观察外形变化来区别 |
7.为达到实验目的,下列实验方案或结论不正确的是( )
| 选项 | 实验目的 | 实验方案或结论 |
| A | 除去铜粉中含有的少量铁粉 | 将混合固体加入到足量稀盐酸中,充分反应后过滤、洗涤、干燥 |
| B | 为了除去粗盐中的Ca2+、Mg2+、SO42-及泥砂,可将粗盐溶于水,然后进行下列五项操作①过滤;②加过量NaOH溶液; ③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液 | 操作顺序是:②④⑤①③ |
| C | 除去CaCl2溶液中的少量稀盐酸 | 加入过量的碳酸钙,过滤 |
| D | 鉴别NaCl溶液、Na2SO4溶液和(NH4)2SO4溶液 | 各取少量于试管中,分别滴加Ba(OH)2溶液,观察现象 |
| A. | A | B. | B | C. | C | D. | D |