题目内容
5.只需要一次实验就能将H2SO4、NaCl、NaOH三种无色溶液区别开来的是( )| A. | 纯碱溶液 | B. | 稀盐酸 | C. | pH试纸 | D. | 酚酞试液 |
分析 根据三种物质与同种试剂反应产生的不同现象来鉴别它们,若两种物质与同种物质反应的现象相同,则无法鉴别它们.
解答 解:A、纯碱溶液与硫酸反应生成二氧化碳气体,与NaCl、NaOH均不反应,不能出现三种明显不同的现象,不能鉴别,故选项错误.
B、稀盐酸与氢氧化钠反应生成氯化钠和水,但无明显变化,与H2SO4、NaCl均不反应,不能出现三种明显不同的现象,不能鉴别,故选项错误.
C、分别用pH试纸测定pH,等于7的是氯化钠溶液,小于7的是硫酸,大于7的是氢氧化钠溶液,能出现三种明显不同的现象,可以鉴别,故选项正确.
D、无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变红色,H2SO4、NaCl、NaOH三种无色分别显酸性、中性、碱性,使酚酞溶液分别显示无色、无色、红色,不能出现三种明显不同的现象,不能鉴别,故选项错误.
故选:C.
点评 本题有一定难度,在解决鉴别物质题时,判断的依据是:所选试剂需要与待鉴别的物质反应并出现明显不同的现象.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
15.将下列食品或生活用品加入水中,能形成溶液的是( )
| A. | 植物油 | B. | 面粉 | C. | 藕粉 | D. | 食盐 |
13. 如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
 如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )| A. | t1℃时,20g a加入到50g水中,充分溶解后得到70ga的饱和溶液 | |
| B. | t2℃时,a、b、c三种物质的溶解度大小关系是a>b>c | |
| C. | t1℃时a、c两物质的饱和溶液中所含的溶质质量一定相等 | |
| D. | t2℃时,将75g的a饱和溶液降温到t1℃,析出30g晶体 |
20.大蒜中含有一种有效成分硫化丙烯(C3H6S)具有杀菌食疗的作用,下列有关硫化丙烯的说法正确的是( )
| A. | 硫化丙烯由3个碳原子、6个氢原子、一个硫原子构成 | |
| B. | 硫化丙烯中碳、氢、硫元素的质量比为3:6:1 | |
| C. | 硫化丙烯中碳的质量分数最大 | |
| D. | 硫化丙烯完全燃烧只生成二氧化碳和水 |
10.据报道,我国科学家首次实现二氧化碳直接加氢制取高辛烷值汽油.汽油是汽车发动机的主要燃料,其主要成分辛烷(X)燃烧反应的化学方程式为2X+25O2$\frac{\underline{\;点燃\;}}{\;}$16CO2+18H2O,则辛烷的化学式为( )
| A. | C2H6 | B. | C6H14 | C. | C8H18 | D. | C16H36 |
14.下列属于复分解反应的是( )
| A. | Fe+CuSO4═FeSO4+Cu | B. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | ||
| C. | H2SO4+2NaOH═Na2SO4+2H2O | D. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 |
15.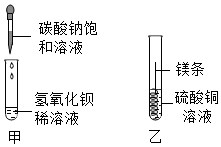 某同学进行如图两个实验:
某同学进行如图两个实验:
(l)甲实验中反应的化学方程式为Ba(OH)2+Na2CO3═BaCO3↓+2NaOH;
(2)乙实验观察到的现象是镁条表面出现红色固体,溶液由蓝色变成无色
(3)把甲、乙反应后的溶液倒入同一烧杯,发现有白色沉淀生成.他决定对白色沉淀的成分进行探究.
【查阅资料】硫酸钡不溶于酸.
【提出猜想】白色沉淀为:Ⅰ.Mg(OH)2;Ⅱ.Mg(OH)2和BaSO4;Ⅲ.Mg(OH)2和MgCO3.
【实验方案】
【拓展与思考】如果猜想Ⅲ成立,产生此结果的原因是做甲实验时滴加的碳酸钠过量;上述白色沉淀的成分不可能出现的组合是Mg(OH)2、MgCO3和BaSO4,原因是甲反应后的溶液中碳酸钠与氢氧化钡不能共存.
 某同学进行如图两个实验:
某同学进行如图两个实验:(l)甲实验中反应的化学方程式为Ba(OH)2+Na2CO3═BaCO3↓+2NaOH;
(2)乙实验观察到的现象是镁条表面出现红色固体,溶液由蓝色变成无色
(3)把甲、乙反应后的溶液倒入同一烧杯,发现有白色沉淀生成.他决定对白色沉淀的成分进行探究.
【查阅资料】硫酸钡不溶于酸.
【提出猜想】白色沉淀为:Ⅰ.Mg(OH)2;Ⅱ.Mg(OH)2和BaSO4;Ⅲ.Mg(OH)2和MgCO3.
【实验方案】
| 实验操作 | 实验现象与结论 |
| 过滤、洗涤白色沉淀备用;向白色沉淀中加入盐酸至过量 | ①若沉淀全部溶解,且无其它现象;猜想Ⅰ成立;其化学反应方程式为Mg(OH)2+2HCl=MgCl2+2H2O. ②若白色沉淀部分溶解且无气体产生,猜想Ⅱ成立. ③若沉淀完全溶解,且有气体产生,猜想Ⅲ成立. |

 如图是A、B、C三种物质的溶解度曲线
如图是A、B、C三种物质的溶解度曲线